 查看详情
查看详情MAH QA岗位职责
药品生产行业,从事药品质量工作的,有个比较特殊的岗位——MAH QA,本人有幸从事过多年,想把一些自己经历的过往经验,同行业中各位有志在此领域发展或者要进行委托生产的企业质量人员进行分享,仅供参考,不足之处,希望见谅。药品生产质量QA,目前行业里划分一般是按照现场QA、体系QA、...
CIO专家-雷丸
 查看详情
查看详情AAV基因治疗药物质量控制策略
基因治疗制品的质量控制策略,应是从早期候选药物筛选阶段到上市后的持续监控的药品整个全生命周期的管理。并基于质量源于设计(QbD)的理念下,从生产工艺开发、生产原辅料选择和检定、生产工艺中间控制、工艺的性能确认和验证、原液成品放行检测、以及产品的表征研究和稳定性研究等方面控制质量风...
CIO专家-无名子
 查看详情
查看详情闲谈新药技术转移
从事药品生产质量多年,期间本人也或多或少接触到了药品经营质量、药品流通质量、警戒质量方面,最近接触到研发质量,特地跟同行们闲聊一下。药品技术转移前端的实验室阶段,质量人员需要做的,基本就是核实数据完整性、真实性、可追溯性。比如实验过程要看一看,对记录、对照品等进行监督;再就是对文...
CIO专家-雷丸
 查看详情
查看详情未获准许就邮寄第二类精神药品,广州1药企被处罚
在医药体制改革升级的大背景下,药品生产/经营的合规性管理问题日益凸显。在动态检查的过程中,药品监管部门对企业的监管重点将渗透到生命周期的各个环节,加强了对事中和事后的监管,NMPA建立专职检查员队伍,对企业进行日常跟踪检查,“飞行检查”已成为常态化。为了帮助医药从业人员更直接了解...
CIO专家-山丹
 查看详情
查看详情真空衰减法检查产品包装密封性的验证及操作注意事项
CDE发表的《化学药品注射剂包装系统密封性研究技术指南(试行)》中,对具有顶空气或充有液体包装的产品,可以使用真空衰减法测试其包装系统的密封性,近几年,因其方法可确定性、设备操作简便、实际指导意义强等,越来越多的注射剂企业开始使用此方法。真空衰减法检查产品包装密封性可以是在研发阶...
CIO专家-岩石松
 查看详情
查看详情无药品经营许可在天猫网店销售药品,广州1药企被罚25万元
在医药体制改革升级的大背景下,药品生产/经营的合规性管理问题日益凸显。在动态检查的过程中,药品监管部门对企业的监管重点将渗透到生命周期的各个环节,加强了对事中和事后的监管,NMPA建立专职检查员队伍,对企业进行日常跟踪检查,“飞行检查”已成为常态化。为了帮助医药从业人员更直接了解...
CIO专家-山丹
 查看详情
查看详情药品技术转移过程中的注意事项
药品的技术转移通常包括生产工艺和分析方法转移,转移能够发生在不同阶段,常见的是:● 生产工艺从研发阶段转入生产阶段;● 分析方法从研发实验室转向企业实验室;● 已上市产品在不同企业间/不同生产场地的转移。特别是近几年MAH制度的执行,技术转移更成为常见的项目。新版药品GMP指南质...
CIO专家-岩石松
 查看详情
查看详情药品生产许可证变更,不是一件简单的事情
药品安全事关人民生命健康,严格把控药品生产质量是关键。药品生产许可证是衡量一个制药企业是否具备合法生产药品的重要标志。在实际生产过程中,药品生产许可证变更的情况也时有发生。本文将通过通俗易懂的方式,为您科普药品生产许可证变更的相关知识。一、什么是药品生产许可证首先,让我们了解一下...
CIO专家-秦艽
 查看详情
查看详情新版药品GMP指南无菌制剂上册变化带来的几点思考
新版无菌制剂结合过去十几年国内外制药行业的具体实践,吸收和借鉴法规指南的关键变化,汇编成比上版增加近一倍内容的指导性指南,给企业带来了福音。本次将无菌制剂上册前后两版进行了详细对比后,个人有一些思考,汇总如下,仅代表个人看法。1.增加并细化了人员管理内容,进一步强调了人员管理的重...
CIO专家-岩石松
 查看详情
查看详情药品生产企业现场检查人员安排及应对策略
药品生产企业人员多、岗位多、流程多,三多是很常见的。在药品现场检查中,涉及的检查涵盖药品生产许可检查、药品注册核查、药品GMP符合性检查、飞行检查等,今天咱们就聊聊现场检查的人员安排及应对策略。所谓养兵千日用兵一时,在现场检查时,最后的临门一脚,所有的精兵强将都得用上啊。详细如下...
CIO专家-岩石松
 查看详情
查看详情AAV基因治疗药物分析技术及挑战
在2012年,欧盟批准了首个的基因治疗药物Glybera(格利贝拉)上市。尽管后来由于商业原因该药物退出了市场,但这一批准意味着基因治疗研发迎来了全新的时代。此后,基因治疗相关的临床试验数量呈爆发性增长的趋势,截至到目前全球基于病毒载体的体内基因疗法14款被批准上市。AAV基因治...
CIO专家-无名子
 查看详情
查看详情提交虚假药师资格证申请经营许可,又有药企被处罚
在医药体制改革升级的大背景下,药品生产/经营的合规性管理问题日益凸显。在动态检查的过程中,药品监管部门对企业的监管重点将渗透到生命周期的各个环节,加强了对事中和事后的监管,NMPA建立专职检查员队伍,对企业进行日常跟踪检查,“飞行检查”已成为常态化。为了帮助医药从业人员更直接了解...
CIO专家-山丹
 查看详情
查看详情以现代物流为例,探讨开办药品批发企业的问题
2005年国家食品药品监管局在《关于加强药品监督管理促进药品现代物流发展的意见》中要求各省推行药品现代流通模式,从监督管理的角度促进药品现代物流较快发展,各省也是推出了相应的准入标准。下面CIO小编从几方面来介绍开办药品批发企业现代物流有哪些需要关注的问题。开办药品批发企业现代物...
CIO专家-爬山虎
 查看详情
查看详情办理药品经营许可证的重要性:检查中的药酒以何界定?
台江区局执法人员联合市公安局台江分局到福州某健康管理有限公司经营场所进行现场检查时发现:当事人在未取得《药品经营许可证》的情况下擅自从事药品经营活动的行为,违反了《药品管理法》第五十一条第一款的规定。根据依据《行政处罚法》第二十八条、《药品管理法》第一百一十五条的相关规定,责令当...
CIO专家-爬山虎
 查看详情
查看详情药品注册生产现场核查应对策略
药品注册生产现场核查一直是重点,漫漫道路已至尾声,企业都不愿在最后出现异常,导致产品注册批件延后或被终止。本文针对药品注册生产现场核查应对措施做出详细分解。法规指南2021年12月20日 CFDI制定公布《药品注册核查工作程序(试行)》等5个文件的通告(2021年第30号)(自2...
CIO专家-岩石松
- 查看详情
以现场核查法规全流程为例讲解药品注册
药品注册申请受理后,药品审评中心(CDE)在药品注册申请受理四十日内通知药品核查中心(CFDI)启动注册核查工作,以核实申报资料的真实性、一致性以及药品上市商业化生产条件,检查药品研制的合规性、数据可靠性等。现在CIO小编对药品注册:注册现场核查流程、核查要点及内容进行总结归纳。...
CIO专家-爬山虎
 查看详情
查看详情GMP符合性检查的经验分享
自从2019年12月1日起,取消药品GMP认证,不再发放药品GMP证书,实现了《GMP证书》和《生产许可证》“两证合一”。《药品生产监督管理办法》(以下简称《办法》)自2020年7月1日起实施,该《办法》第二十六条规定:“从从事药品生产活动,应当遵守药品生产质量管理规范,建立健全...
CIO专家-爬山虎
 查看详情
查看详情了解FDA药品注册的关键步骤
FDA是美国药品食品管理局的简称。 主要是针对药品,化妆品,医疗器具械,食品饮料,激光类产品等的认证。这里主要讲一下原料药注册。美国是世界第一大的药品生产和销售的市场,药品可以进入美国市场销售是众多制药企业所共同憧憬的目标,注册审批是药品进入美国市场的重要环节,是敲门砖,更是药品...
CIO专家-爬山虎
 查看详情
查看详情药品网络销售退货处理浅析
随着电商的普及,药品网络销售也得到了迅猛发展。各种问题随之而来。本文主要剖析药品网络销售过程中有关退货处理问题。网络销售退货,主要有以下几种情况:一、产品质量问题1.顾客收到货后,反映产品被破坏,如产品包装炸裂、产品包装变形、漏液,产品断裂(如药片被挤压变成两半)因而要求退货;2...
CIO专家-海龙
 查看详情
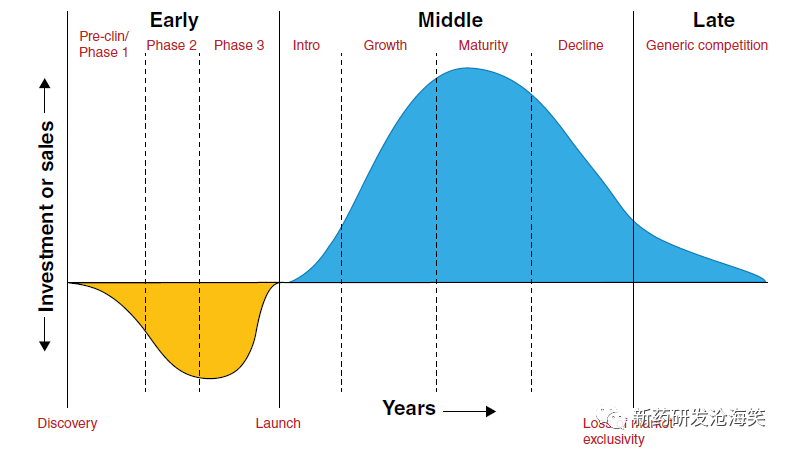
查看详情创新药生命周期管理-Why?What?How?
引言在当今竞争激烈、不断变化的制药市场环境中,品牌药物所有者越来越致力于开发综合生命周期管理策略,以实现其产品组合中每种产品的最大收益,并确保其继续能够找到将为更多患者带来实际效益的新治疗方法。不同的产品和市场的生命周期将有所不同。本文回答创新药的生命周期的三个问题:Why?Wh...
CIO专家-山丹





