基本信息
1、办理部门:上海市药品监督管理局
2、办理方式:窗口办理,网上办理,快递申请
3、办理地点:上海市徐汇区虹梅路街道宜山路728号3号楼底楼大厅上海市药品监督管理局行政服务中心1-5号窗口
4、咨询电话:021-63269368 CIO咨询:400-003-0818
受理条件
申请材料齐全,符合法定形式,具体见申请材料目录。
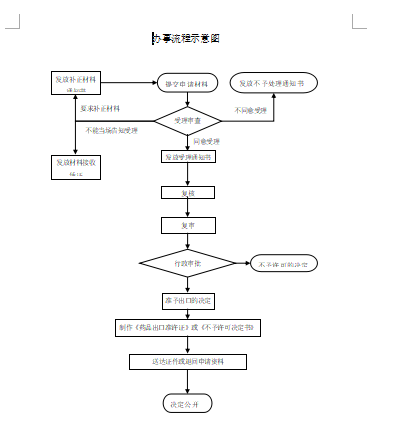
办理流程
流程文字说明
1、申请:申请人通过省政务服务网网上申报,并提交相关电子申请材料。申请人按照申报资料要求,提供一套纸质材料,通过邮寄或直接递交,或者委托相关人员递交省药品监督管理局受理大厅。
2、受理:5个工作日。
申请材料齐全,符合法定形式,具体见申请材料目录。
3、审查与决定:15个工作日。
特别程序:行政审查。
准予批准的条件:(1)申请人为本市行政区域内有关的药品生产、进出口企业;(2)申请出口的产品属于兴奋剂中的蛋白同化制剂及肽类激素;(3)出口产品如为境内企业接受境外企业委托生产的品种,必须签订委托生产合同,明确产品质量由委托方负责;(4)审批申请提交的资料和程序符合相关法律法规要求。
4、颁证与送达:10个工作日。
直接送达、邮寄送达、公告送达。
申请材料
1、药品出口申请表;>>药品出口申请表
2、进口国家或地区的药品管理机构提供的进口准许证正本(或者复印件及公证文本)。如进口国家或地区对蛋白同化制剂、肽类激素进口尚未实行许可证管理制度,需提供进口国家的药品管理机构提供的该类药品进口无需核发进口准许证的证明文件(正本)以及以下文件之一: (1)进口国家或地区的药品管理机构提供的同意进口该药品的证明文件正本(或者复印件及公证文本);(2)进口单位合法资质的证明文件和该药品用途合法的证明文件正本(或者复印件及公证文本);
3、出口药品如为国内生产企业经批准生产的品种,须提供该药品生产企业的《药品生产许可证》、《企业法人营业执照》及药品批准证明文件;出口药物如为境内企业接受境外企业委托生产的品种,须提供与境外委托企业签订的委托生产合同。委托生产合同应当明确规定双方的权利和义务、法律责任等,产品质量由委托方负责;
4、出口企业的《企业法人营业执照》、《进出口企业资格证书》(或《对外贸易经营者备案登记表》)、《组织代码证书》;
5、购货合同或者订单复印件(自营产品出口的生产企业除外);
6、外销合同或者订单复印件;
7、《营业执照》或《事业单位法人证书》;
8、经办人身份证明。
结果样本

常见问题
问题1:蛋白同化制剂、肽类激素出口准许证新办的准予批准的条件?
答:申请企业应当符合以下条件:(1)申请人为本市行政区域内有关的药品生产、进出口企业;(2)申请出口的产品属于兴奋剂中的蛋白同化制剂及肽类激素;(3)出口产品如为境内企业接受境外企业委托生产的品种,必须签订委托生产合同,明确产品质量由委托方负责;(4)审批申请提交的资料和程序符合相关法律法规要求。
本办事指南摘自药监局官网,如有变动,以官方发布为准。