基本信息
1、办理部门:安徽省药品监督管理局
2、办理方式:网上办理、窗口办理
3、办理地点:安徽省合肥市包河区马鞍山路509号安徽省政务服务中心1号办事大厅企业开办综合窗口
4、咨询电话:0551-62999253、0551-62999793 CIO咨询:400-003-0818
受理条件
申办者应当在试验项目经伦理审查通过并与临床试验机构签订协议或合同。
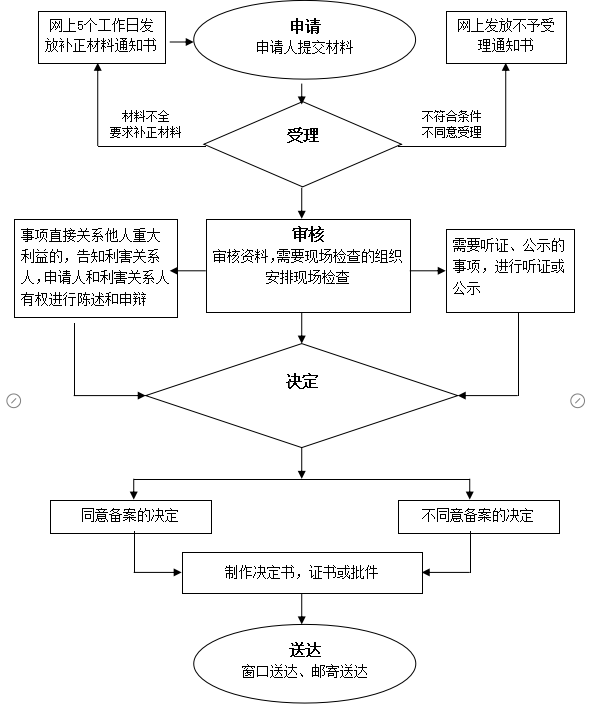
办理流程
流程文字说明
法定办理时限:1个工作日;承诺办理时限:1个工作日
1、受理(时限:0.25个工作日)
2、审查(时限:0.25个工作日)
3、决定(时限:0.25个工作日)
4、办结(时限:0.25个工作日)
申请材料
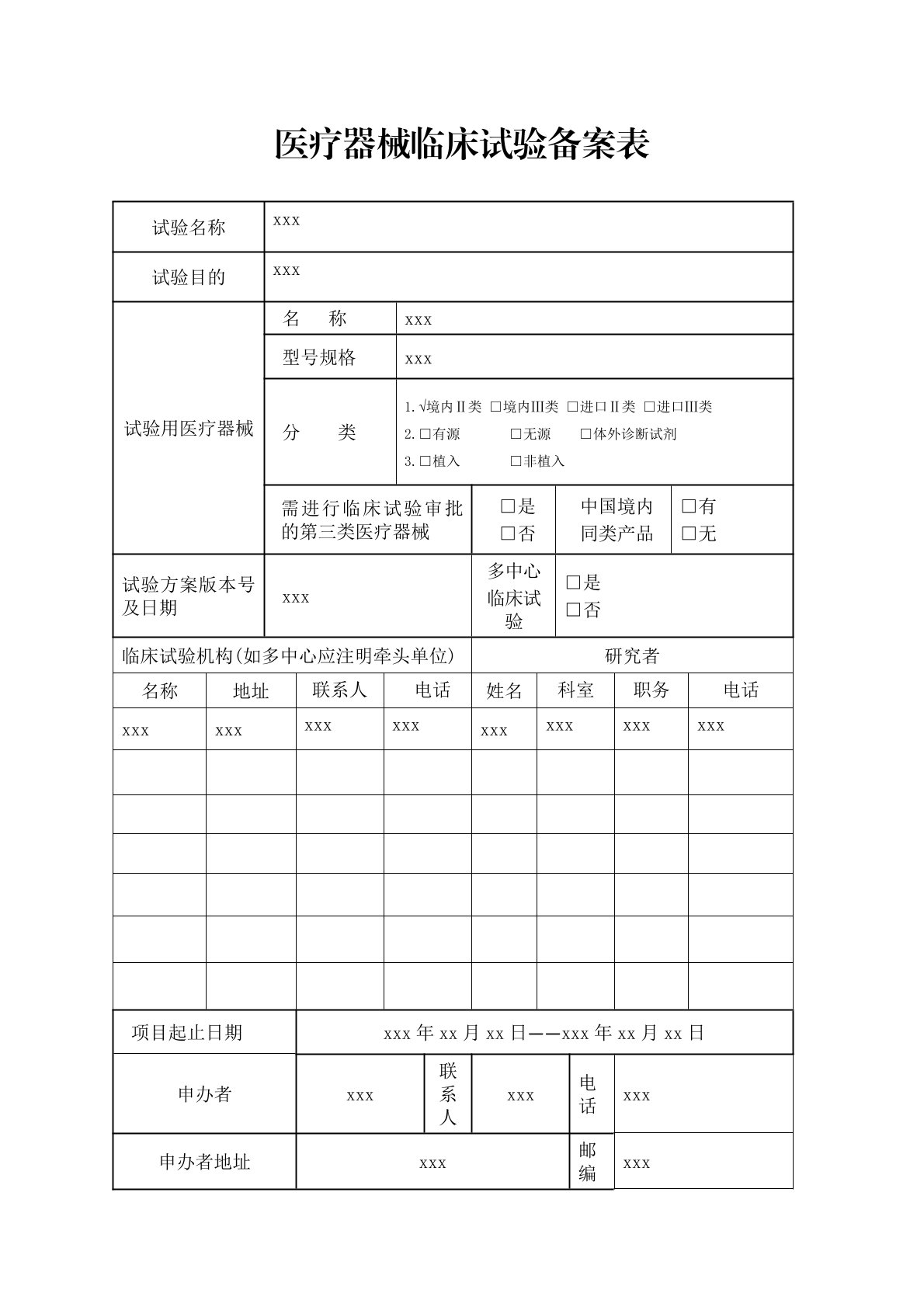
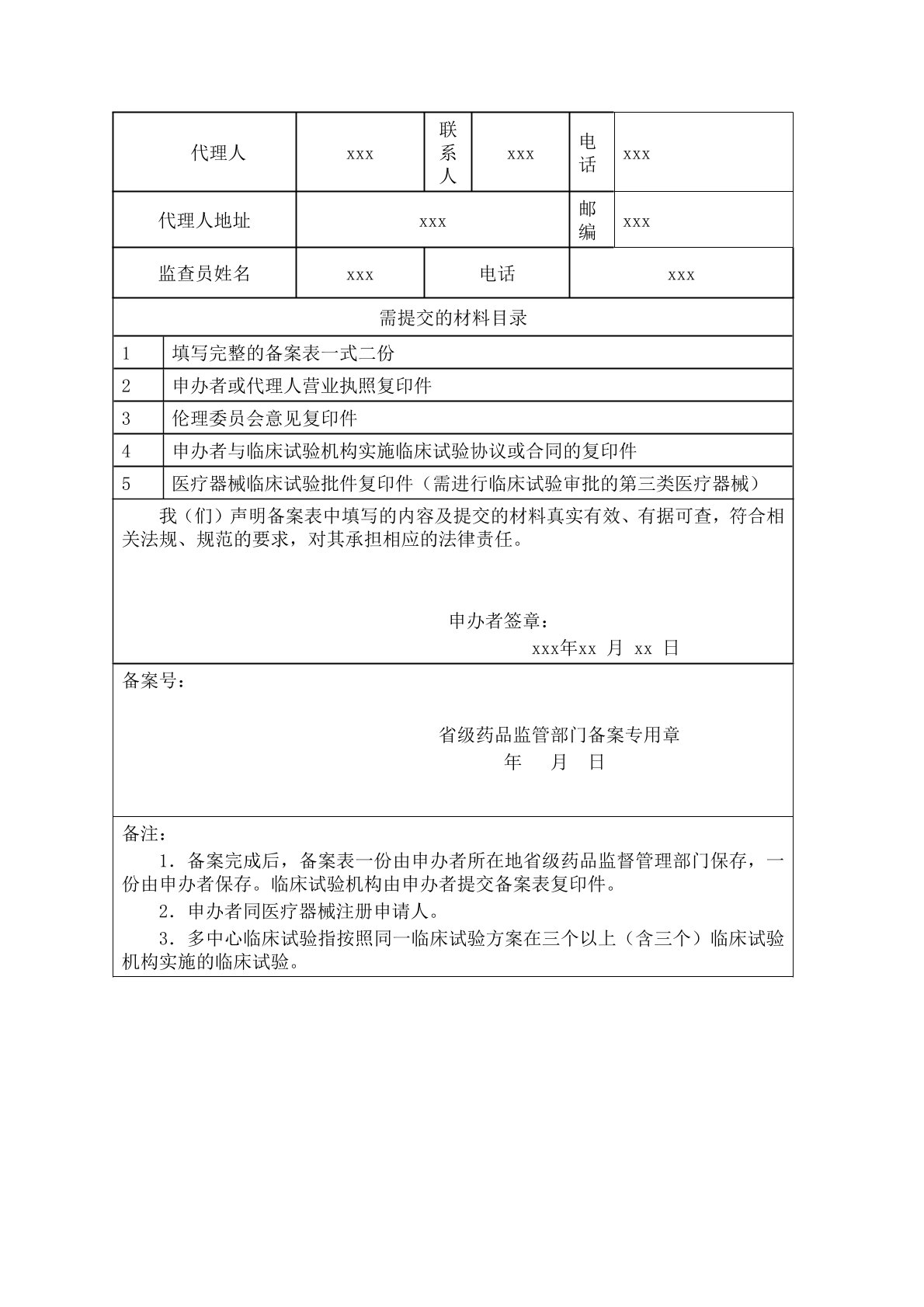
1、医疗器械临床试验备案表;
2、营业执照;
3、伦理委员会意见;
4、申办者与临床试验机构实施临床试验协议或合同;
5、医疗器械临床试验批件。
结果样本
常见问题
问题1:申办者应向哪个部门申请医疗器械临床试验备案?
答:境内医疗器械向申办者所在地省级药品监督管理部门备案,进口医疗器械向代理人所在地省级药品监督管理部门备案。
问题2:列入需进行临床试验审批的第三类医疗器械目录的临床试验产品如何开展临床试验?
答:列入需进行临床试验审批的第三类医疗器械目录的,还应当获得国家药品监督管理局的批准,并且在符合要求的三级甲等医疗机构实施临床试验。
问题3:多中心临床试验的定义?
答:多中心临床试验是指按照同一临床试验方案,在两个以上(含两个)医疗器械临床试验机构实施的临床试验。
本办事指南摘自药监局官网,如有变动,以官方发布为准。
























