基本信息
1、办理部门:安徽省药品监督管理局
2、办理方式:网上办理、窗口办理
3、办理地点:安徽省合肥市包河区马鞍山路509号安徽省政务服务中心1号办事大厅企业开办综合窗口
4、咨询电话:0551-62999882、0551-62999795 CIO咨询:400-003-0818
受理条件
1. 申请人为持有安徽省药品监督管理局核发的药品生产许可证,并有原料药出口欧盟的的药品生产企业。
2. 申请材料(具体见申请材料目录)齐全、符合形式审查要求,或者申请人按照要求提交全部补正材料的,予以受理。
3. 取得我国《药品生产许可证》企业生产的具有药品批准文号的原料药(通过GMP符合性检查)对应的为1-8项材料。
4. 取得我国《药品生产许可证》企业生产的尚未取得药品批准文号的原料药(包括有原料药批准文号,但尚未通过药品GMP符合性检查的品种)对应的为1-3、7-11项材料。
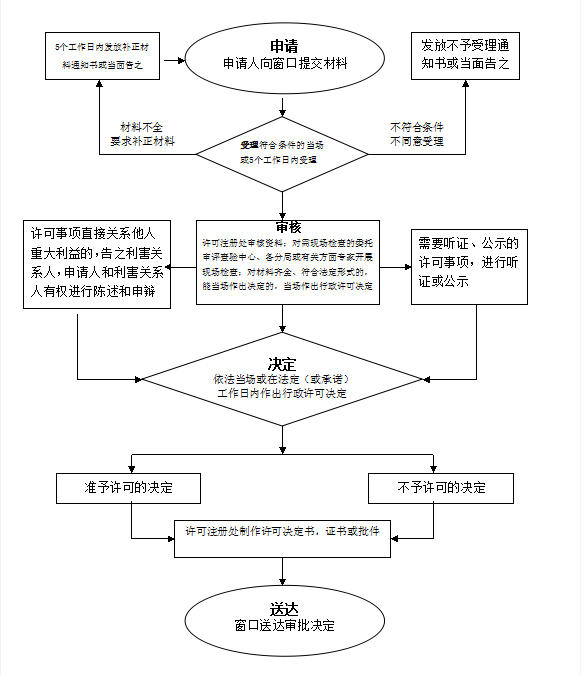
办理流程
流程文字说明
法定办理时限:20个工作日;承诺办理时限:20个工作日
1、受理(时限:1个工作日)
2、审查(时限:17个工作日)
3、决定(时限:1个工作日)
4、办结(时限:1个工作日)
申请材料
1、出口欧盟原料药证明文件申请书;
2、药品生产许可证;
3、营业执照;
4、我国药品监管部门发给的药品批准证明文件;
5、该品种通过中国药品GMP符合性检查的文件材料;
6、监管部门最近一次对其药品GMP符合性检查意见整改情况;
7、该品种近3年通过其余国家或组织的药品GMP检查的文件材料;
8、该品种与国外采购企业的销售合同;
9、药品生产工艺;
10、药品质量标准;
11、三批样品自检报告。
结果样本


常见问题
问题1:网上上传的资料需要逐页盖章吗?
答:需要。
问题2:是否需要现场检查?
答:已取得国内药品注册批件且通过GMP符合性检查的,无需检查。
问题3:文件有效期是多少?
答:3年。
本办事指南摘自药监局官网,如有变动,以官方发布为准。
























