基本信息
1、办理部门:江苏省药品监督管理局
2、办理方式:网上办理
3、办理地点:南京市建邺区汉中门大街145号江苏省政务服务中心省药监局窗口
4、咨询电话: 12315 CIO咨询:400-003-0818
受理条件
《中华人民共和国行政许可法》第三十二条第五项: 申请事项属于本行政机关职权范围,申请材料齐全、符合法定形式,或者申请人按照本行政机关的要求提交全部补正申请材料的,应当受理行政许可申请。
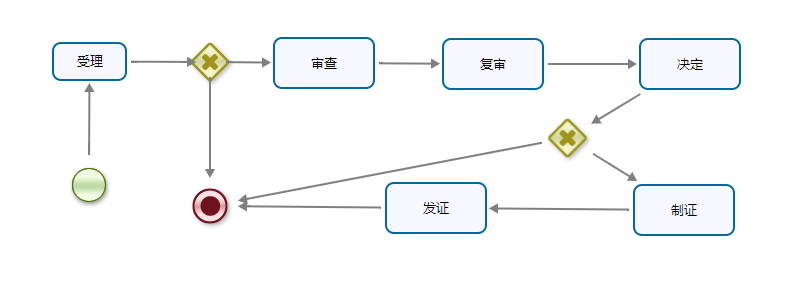
办理流程
流程文字说明
1、审查、决定(时限:20个工作日)
办理结果:初审意见。
申请材料
1、创新医疗器械特别审查申请表;>>创新医疗器械特别审查申请表
2、申请人企业资质证明文件;
3、产品知识产权情况及证明文件;
4、产品研发过程及结果的综述;
5、产品技术文件;
6、产品创新的证明性文件;
7、产品安全风险管理报告;
8、产品说明书(样稿);
9、其 他证明产品符合国家药品监督管理局发布的《创新医疗器械特别审查程序》第二条要求的资料;
10、资料真实性的自我保证声明。>>承诺书
结果样本

常见问题
问题1:关于创新医疗器械特别审查程序中有关专利方面有哪些要求?
答:创新医疗器械的审查条件之一就是申请人在中国依法拥有产品核心技术发明专利权。考虑存在核心技术发明专利的申请已由国务院专利行政部门公开,但最终未被授予专利权的情况,因此增加对产品核心技术方案的预评价。
国家知识产权局专利检索咨询中心是国家知识产权局直属单位,申请人可向专利检索咨询中心提出检索申请。
为进一步鼓励创新,激发医疗器械生产企业的研发活力,考虑到专利的特点与医疗器械研发的平均周期,因此,确定创新医疗器械特别审查申请时间距专利授权公告日不超过5年。
本办事指南摘自药监局官网,如有变动,以官方发布为准。