基本信息
1. 办理部门:浙江省药品监督管理局
2. 办理方式:网上申请
3. 办理地点:浙江省药品监督管理局行政审批事项受理大厅(杭州市西湖区西溪街道)
4. 药监咨询:0571-88903246-1 CIO咨询:400-003-0818
受理条件
(一)医疗器械临床试验项目经伦理审查通过且申办者(即医疗器械注册申请人或代理人)与临床试验机构签订协议或合同。
(二)按要求提交规定的申请材料并符合要求。
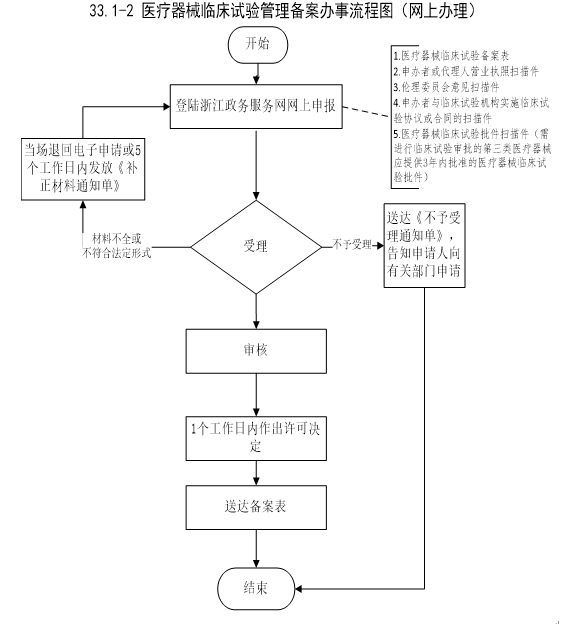
办理流程
流程文字说明
1、申请
申请人通过省政务服务网网上申报,并提交相关电子申请材料。申请人按照申报资料要求,提供一套纸质材料,通过邮寄或直接递交,或者委托相关人员递交省药品监督管理局受理大厅。
2、受理(时限:1个工作日)
办理结果:(1)申请事项依法不属于本行政机关职权范围的出具不予受理通知书;
(2)材料不齐全或者不符合法定形式,一次性告知补正的全部材料,送达《补正申请材料通知书》;
(3)申请材料齐全并且符合法定形式,予以受理并送达《受理通知书》。
3、审查和决定(时限:当场办结)
办理结果:(1)申请人的申请材料符合法定条件,标准、审核通过的,出具核准、审批文件。(2)申请人的申请材料不符合法定条件、标准,审核不通过的,出具不予核准、审批文件。
4、送达(时限:10个工作日)
办理结果:送达审批文件。
申请材料
1、医疗器械临床试验审批意见单;
2、伦理委员会意见扫描件;
3、医疗器械临床试验备案表;
4、申办者及代理人营业执照扫描件;
5、申办者与临床试验机构实施临床试验协议或合同的扫描件。
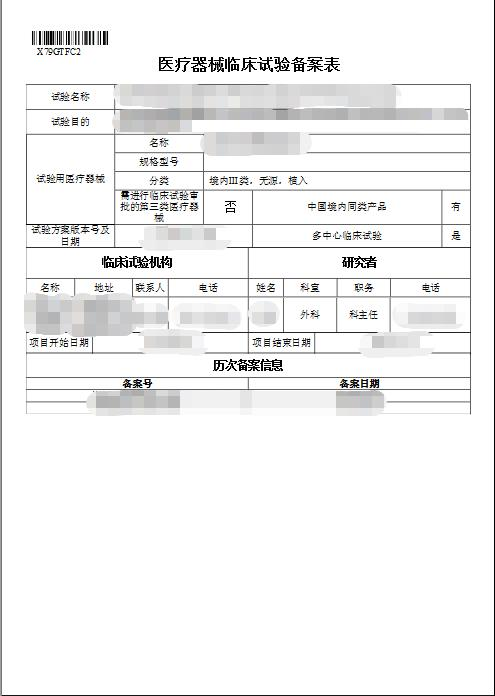
结果样本
常见问题
问题1:申办者或代理人完成临床试验备案后,试验项目起止日期发生变化是否需要申请变更?
答:申办者或代理人完成临床试验备案后,试验项目起止日期有变化的,应当于变化后10个工作日内提交书面情况说明(加盖申办者公章)。
本办事指南摘自药监局官网,如有变动,以官方发布为准。