
跟踪检查不符合GMP,数家药企被责令停产!
发布时间:2022-03-22 收藏
详情介绍
该案例下关联内容:
培训:药品生产企业合规管理七招
案例解析
2月22日,江苏省药监局发布一则药品生产企业风险控制措施公告
公告显示,2021年11月28日-30日
对某药企进行跟踪检查时
发现该企业硬胶囊剂不符合药品生产质量管理相关规定
根据《药品管理法》第九十九条及
《药品生产监督管理办法》第五十九条规定
决定暂停该企业硬胶囊剂的生产
而值得注意的是,近几个月来
已有数家药企因存在缺陷而被责令停产了
其中比较典型的是

某制药企业的格列美脈片,在飞检中检查出
存在严重缺陷2项,主要缺陷2项
被责令立即暂停格列美脈片的生产和销售
而又因该品种属于第二批国家集采品种
该企业的格列美脈片也因此被国家联采办取消了中选资格
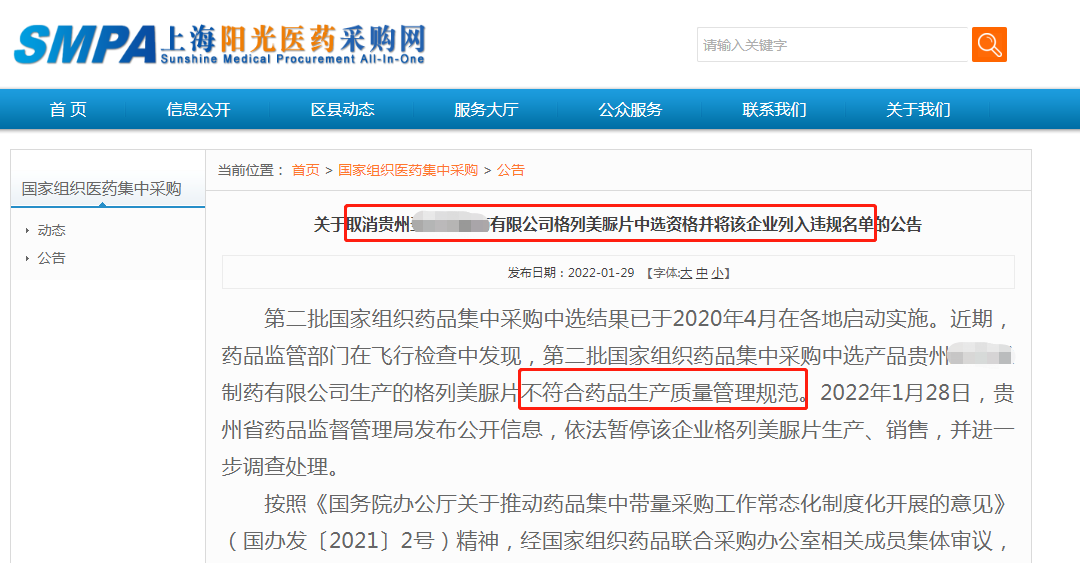
并暂停了企业2022年1月29日至2023年7月28日
参与国家组织药品集中采购活动的申报资格
简直是,稍不注意就容易满盘皆输
在生产经营活动中
药企需时面临抽检、飞行检查、日常检查等监管
一旦被查处违规导致停产
势必会对企业的发展造成影响
合规合法生产经营才是企业生存的第一守则
除此之外
CIO也为企业提供GMP符合性检查合规审计服务
现场审计,排查风险点,出具报告
为贵司合规生产护航
联系我们,了解详情
2月22日,江苏省药监局发布一则药品生产企业风险控制措施公告公告显示,2021年11月28日-30日对某药企进行跟踪检查时发现该企业硬胶囊剂不符合药品生产质量管理相关规定根据《药品管理法》第九十九条及《药品生产监督管理办法》第五十九条规定决定暂停该企业硬胶囊剂的生产而值得注意的是,近几个月来已有数家药企因存在缺陷而被责令停产了其中比较典型的是Commented [A1]:说某制药企业的格列美脈片,在飞检中检查出存在严重缺陷2项,主要缺陷2项被责令立即暂停格列美脈片的生产和销售而又因该品种属于第二批国家集采品种该企业的格列美脈片也因此被国家联采办取消了中选资格并暂停了企业2022年1月29日至2023年7月28日参与国家组织药品集中采购活动的申报资格简直是,稍不注意就容易满盘皆输在生产经营活动中药企需时面临抽检、飞行检查、日常检查等监管一旦被查处违规导致停产势必会对企业的发展造成影

药械企业法律风险预防与应对闭门会

执业药师继教服务

合规破局与价值重塑 医药营销转型实战训练营

药物警戒第三方委托服务

医药企业涉刑防范与应对

生死红线——「医改+反腐」背景下的医药企业生存逻辑与增长路径企业内训

药品医疗器械企业安全风险排查服务

【医药传播】药企品牌 / 产品宣传片制作

医疗器械注册/备案、变更

药品(国产/进口)注册、变更

药品经营许可申请 / 变更

化妆品生产许可申请/变更

医疗器械生产许可申请/变更

药品上市许可持有人的B证申请

药品生产许可申请 / 变更(药厂筹建)

原辅包注册/登记

化妆品注册/备案、变更

药械企业法律风险预防与应对闭门会

执业药师继教服务

合规破局与价值重塑 医药营销转型实战训练营

药物警戒第三方委托服务

医药企业涉刑防范与应对

生死红线——「医改+反腐」背景下的医药企业生存逻辑与增长路径企业内训




