广东省中药饮片抽检不合格原因分析
CIO专家-干姜
近日广东省药监局发布了药品抽查检验信息的通告(2021年第9期),11个品种1813批次经检验符合药品标准规定,毫无意外的是不合格品种几乎全部为中药饮片,具体信息如下:
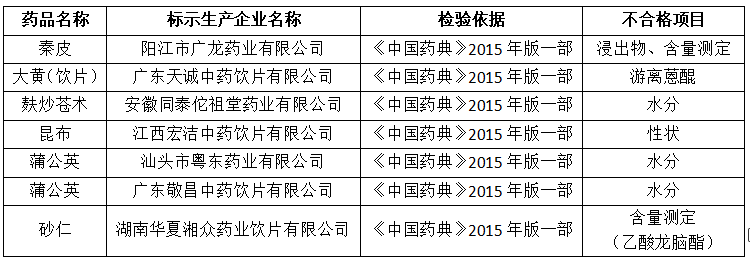
有人问为何各省市的抽检不合格多数为中药饮片,个人觉得原因有二:
第一,药品管理法第一百一十七条:生产、销售劣药的,处违法生产、销售的药品货值金额十倍以上二十倍以下的罚款,金额不足十万元的,按十万元计算;生产、销售的中药饮片不符合药品标准,尚不影响安全性、有效性的,责令限期改正,给予警告;可以处十万元以上五十万元以下的罚款。
从条款我们可以看出,因为处罚力度大所以制剂企业自身的把控也就更严格,市面上不合格的制剂就少,这是间接造成如今饮片行业抽检不合格占比居高不下的一个原因。
何为尚不影响安全性、有效性的,广东省已给出明确答复,有兴趣的朋友可以仔细阅读下,《广东省药品监督管理局中药饮片不符合药品标准尚不影响安全性、有效性的认定指导原则》解读:
1.二氧化硫残留量、重金属及有害元素、农药残留量、真菌毒素、直接口服及泡服饮片的微生物限度、毒性成分的限量检查等项目不符合标准时通常认定为影响中药饮片安全性。
2.鉴别、浸出物、特征图谱/指纹图谱、含量测定等项目不符合标准时通常认定为影响中药饮片有效性。
3.性状、水分或干燥失重、总灰分、酸不溶性灰分、杂质等项目不符合标准时可考虑认定为不影响安全性、有效性”。
第二,中药饮片企业小、乱、杂是这个行业的现状,也是制约行业形成规模化、品牌化的束缚,更是这行业提升GMP管理水平,走向国际市场化的最大障碍。
一直以来中药饮片企业的GMP管理都是令人担忧的,GMP管理游走在法规边缘、打一枪换个地的皮包公司不在少数。
更有企业长期执行外购饮片分包装或改换包装标签、检验数据造假、检验样品造假、炮制工艺违规、编写批生产检验记录等造假行为,这是造成如今饮片行业抽检不合格占比居高不下的另一个原因。
本次抽检不合格的企业可以认定为自身把控不严、GMP管理出现问题,抛开主观造假的影响可以总结为以下几点:
秦皮的浸出物是热浸法,乙醇做溶剂,乙醇浓度、称样量、定容体积的选择是否会影响最终结论。
【浸出物】照醇溶性浸出物测定法(通则2201)项下的热浸法测定,用乙醇作溶剂,不得少于8.0%。
热浸法 取供试品约2~4g,精密称定,置100~250ml的锥形瓶中,精密加水50~100ml,密塞,称定重量,静置1小时后,连接回流冷凝管,加热至沸腾,并保持微沸1小时。放冷后,取下锥形瓶,密塞,再称定重量,用水补足减失的重量,摇匀,用干燥滤器滤过,精密量取滤液25ml,置已干燥至恒重的蒸发皿中,在水浴上蒸干后,于105℃干燥3小时,置干燥器中冷却30分钟,迅速精密称定重量。除另有规定外,以干燥品计算供试品中水溶性浸出物的含量(%)。
秦皮、砂仁和大黄的含量测定,是否评估过取样代表性(留样数据、均匀性等)、检验操作规范性、检验数据真实性可靠性。
麸炒苍术、蒲公英和昆布,性状不合格只能说明企业在验收制度把控不严或对以上情况熟视无睹,水分不合格需要考虑包装形式或提高出厂内控标准。
综合来说,麸炒苍术、昆布、蒲公英可能被认定为尚不影响安全性、有效性从轻处罚,但是秦皮、大黄(饮片)、砂仁的处罚就会相对较重。
对于企业来说,如何构建一个有效的管理体系切实有效的将GMP要求贯彻执行是一项长期的规划,也是企业发展道路上不可或缺的重要部分。
相关文件下载、服务及学习课程:
合规文库:药品GMP基础知识培训
合规培训:限免-药品生产现场管理培训
合规服务:GMP符合性检查
联系专家,获取专家指导意见:e邀专家
最新推荐
热门观点

MAH申请
1.加快研发机构实现批文产品上市。 2.帮助医药公司实现批文产品转让。 3.协助药企实现受托生产。

药厂筹建
1.提供GMP药厂全套解决方案。 2.解决客户关于建设符合GMP要求的药厂的若干问题。 3.帮助顺利筹建药厂。

药品生产许可证A证核发申请
辅导企业完善硬件、软件, 整理生产、注册资料,提交申请,获得《药品生产许可证》(A 证)。

GMP合规审计/GMP认证
1.为企业提供药品gmp审计/GMP认证服务。 2.帮助企业熟悉GMP符合性检查流程。 3.帮助企业顺利通过药品生产质量管理体系审核。

医疗器械GMP体系考核
服务于二类、三类医疗器械生产企业。CIO为医疗器械生产企业提供专业的、定制化质量管理体系,提高产品的质量管理,避免投资浪费,让企业在时效内快速性通过质量体系考核,加快产品上市历程。

化妆品注册备案
1.提供国产/进口特殊/普通化妆品注册备案服务。 2.帮助工厂及贸易商快捷高效的完成注册备案,助力产品上市。

化妆品生产许可证申请
1.提供《化妆品生产许可证》新开办、变更、延续办理业务。 2.诚信经营、正规辅导拿证。 3.提交需求获取服务报价。

药品上市许可转让
对于新药法实施下,药品上市许可持有人可以转让药品上市许可,为企业申请转让批文、收购批文提供一站式服务指导。

药品经营许可证(批发、零售连锁总部)核发
1.开办药品批发、药品零售连锁总部企业,需向所在地省级药品监督管理部门申请,取得《药品经营许可证》。 2.CIO辅导药品零售连锁企业总部筹建和验收,帮助企业顺利拿证。

医疗器械注册证办理服务
1.CIO提供国内/进口二类医疗器械注册办理一站式服务。 2.CIO提供国内/进口三类医疗器械注册办理一站式服务。

药品GSP模拟飞检
上门全面审计企业合规风险,指导企业整改提高; 赶在飞检之前指导企业彻底整改缺陷; 大大降低被飞检停产、撤证的几率。

药品GSP年度服务
药品经营基础课程体系; 每月两次以上更新课程; 每周一次在线集中答疑。

医疗器械GMP年度服务
器械生产基础课程体系; 每月两次以上更新课程; 每周一次在线集中答疑。

医疗器械模拟GMP飞检
上门全面审计企业合规风险,指导企业整改提高; 赶在飞检之前指导企业彻底整改缺陷; 大大降低被飞检停产、撤证的几率。

FDA审计服务/FDA认证
为客户提供全方位的FDA审计咨询、准备与实施,以确保企业顺利通过审计并顺利进入美国市场。

医疗机构制剂注册备案
1.CIO为医疗机构配制制剂提供一站式合规服务。 2.帮助医疗机构取得医疗机构制剂注册批件。 3.价格合理,服务更省心。

药品生产许可证B证核发
1.药品上市许可持有人取得药品批文后,委托生产的,需办理药品生产许可证B证才能合法上市销售。 2.CIO提供药品生产许可证办理业务,帮助您的批文产品尽快上市。

医疗器械互联网信息服务备案
自2025年1月20日起,国家药监局将“药品、医疗器械互联网信息服务审批”改为备案管理。我们为自建网站或平台销售医疗器械的企业提供专业的医疗器械互联网信息服务备案咨询服务,帮助企业高效完成备案。

药品互联网信息服务备案
自2025年1月20日起,药品和医疗器械互联网信息服务审批不再需要前置审批,转而实行备案管理。我们致力于为药企提供高效、专业的药品互联网信息服务备案服务,帮助客户顺利开展网络销售业务。

MAH申请
1.加快研发机构实现批文产品上市。 2.帮助医药公司实现批文产品转让。 3.协助药企实现受托生产。

药厂筹建
1.提供GMP药厂全套解决方案。 2.解决客户关于建设符合GMP要求的药厂的若干问题。 3.帮助顺利筹建药厂。

药品生产许可证A证核发申请
辅导企业完善硬件、软件, 整理生产、注册资料,提交申请,获得《药品生产许可证》(A 证)。

GMP合规审计/GMP认证
1.为企业提供药品gmp审计/GMP认证服务。 2.帮助企业熟悉GMP符合性检查流程。 3.帮助企业顺利通过药品生产质量管理体系审核。

医疗器械GMP体系考核
服务于二类、三类医疗器械生产企业。CIO为医疗器械生产企业提供专业的、定制化质量管理体系,提高产品的质量管理,避免投资浪费,让企业在时效内快速性通过质量体系考核,加快产品上市历程。

化妆品注册备案
1.提供国产/进口特殊/普通化妆品注册备案服务。 2.帮助工厂及贸易商快捷高效的完成注册备案,助力产品上市。






