 E邀专家
E邀专家
自2019年新版《药品管理法》、《疫苗管理法》实施以来,我国医药行业出现了巨大的转变。医药行业是国民经济的重要组成部分,能够直接影响公众的健康安全,尤其是近期国家药监部门发布了《药品经营和使用质量监督管理办法》(征求意见稿),再次证实了监管部门对整治药品经营环节质量安全保障的决心。
经营环节是药品质量保证的中间环节,也是涉及范围最广的领域,药品从生产企业出厂后即进入经营环节,包括了药品的采购、验收、入库、储存、养护、出库、运输、售后等一系列流程,温湿度、外界环境等各类因素都有可能影响到药品本身的质量,因此,保证经营环节的药品质量尤为重要。
首先,目前众多的研究都指出,选取科学有效的决策方法和管理工具,可以有效支持药品质量的监管工作。其次,通过使用工具,推测药品在经营环节可能出现的质量问题,设计有效的决策方法,形成完整的经营环节质量监督计划方案,当实际发生某类质量问题时,直接选取相应的决策方法来解决,能够在很大程度上节约时间成本,产生直接经济和社会效益。经过反复多次地使用该工具,便可以形成成熟且有效的解决问题的方法,从而建立起一套完整的针对某环节的管理决策。在这样一个前提下,使用质量管理工具就是解决采购环节可能存在的药品质量问题的一种方式。
1.质量管理工具的介绍
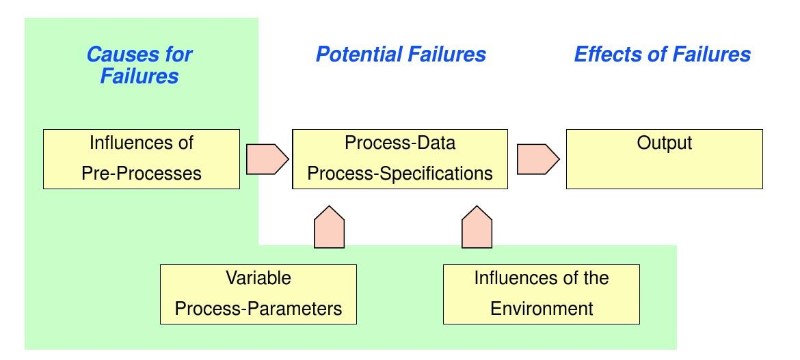
FMEA(FailureModeandEffectAnalysis,失效模式和效果分析)工具是质量管理领域的经典工具,最早是由美国国家宇航局(NASA)形成的一套分析模式,是一种实用的解决问题的方法,用于分析系统或流程所有可能产生的失效模式(故障模式)及对系统造成的可能影响,并按每个失效模式的严重程度等予以分类的一种归纳分析方法,适用于许多工程领域。
FMEA的目的是:
(1)确定过程中潜在失效后果;
(2)确定对可消除或减少潜在失效模式发生机会的措施;
(3)确定过程变量以此聚焦于过程控制。
FMEA实施的重要因素是时效性,它可以细化流程,识别出流程中的薄弱环节,属于事前预防的一种措施。
2.质量管理工具的应用
在药品采购环节使用FMEA工具的目的很重要,需要预先通过多种途径,整理好后续可能出现的问题,这些途径的汇总则应采用经验总结、问卷调研结合的方式,尽可能考虑到所有采购药品时会发生的情形,并归纳每种情形的处理方式,最终形成一套完整的FMEA分析表。
例如,可以假设采购时出现了未审核首营企业资质这一情形,按照FMEA管理工具实施以下步骤:
(1)成立解决问题的小组,成员可以包括质量管理负责人、质量管理部门负责人、质量管理部门工作人员、采购部门负责人、采购部门工作人员等。
(2)描述问题:采购时未审核首营企业资质材料。
(3)问题产生的可能原因:采购负责人、采购工作人员未严格履行审核职责。
(4)问题产生后可能出现的后果:有可能导致假药、劣药进入合格药品仓库并流入药品市场,最终造成公众使用假药或劣药,损害公众健康安全。
(5)解决问题的方式:
①对采购负责人、采购工作人员加以专业知识、素质教育的培训,强化不合格药品有可能给社会大众造成的伤害和一系列法律责任的承担。
②加强采购端口的资质审核制度,严格执行采购的信息化制度,实施首营企业档案制,并辅以双人复核。
③给予采购环节激励-惩罚政策,参照新版《药品管理法》的处罚到人责任制,也可以考虑在本企业实施处罚到人制度,以此加大威慑力,避免后续可能出现的问题。
持续质量改进是药品企业永恒的主题,随着企业经营运作管理的不断更新,药品质量的风险发生频度、可检测度及严重程度等也是在不断变化,因此,企业要在不断变化的过程中,改进优化,及时采取措施降低各种可能存在的风险,将产品做到更好,从而提升企业的经济效益及社会效益,这是FMEA管理的最终目的。适时使用质量管理工具能够较好地提升医药行业的监管效能,稳步提高药品质量保障水平,维护公众用药权益,构建社会主义和谐社会,推动医药行业不断取得新进展。
相关文件下载、服务及学习课程:
合规文库:药品经营企业首营资料管理图谱(药品质量管理员工具)
合规培训:在线答疑第一期-药品经营企业首营资料管理
合规服务:GSP合规审计
联系专家,获取专家指导意见:e邀专家
 E邀专家
E邀专家
最新推荐
热门观点

药械企业法律风险预防与应对闭门会

执业药师继教服务

合规破局与价值重塑 医药营销转型实战训练营

药物警戒第三方委托服务

医药企业涉刑防范与应对

生死红线——「医改+反腐」背景下的医药企业生存逻辑与增长路径企业内训

药品医疗器械企业安全风险排查服务

【医药传播】药企品牌 / 产品宣传片制作

医疗器械注册/备案、变更

药品(国产/进口)注册、变更

药品经营许可申请 / 变更

化妆品生产许可申请/变更

医疗器械生产许可申请/变更

药品上市许可持有人的B证申请

药品生产许可申请 / 变更(药厂筹建)

原辅包注册/登记

化妆品注册/备案、变更

药械企业法律风险预防与应对闭门会

执业药师继教服务

合规破局与价值重塑 医药营销转型实战训练营

药物警戒第三方委托服务

医药企业涉刑防范与应对

生死红线——「医改+反腐」背景下的医药企业生存逻辑与增长路径企业内训






