基本信息
1. 办理部门:浙江省药品监督管理局
2. 办理方式:网上申请,现场窗口申请,邮寄申请
3. 办理地点:企业所在地药品监督管理部门
4. CIO咨询:400-003-0818
受理条件
1、化妆品生产企业生产条件发生变化,不再符合化妆品生产质量管理规范要求。
2、化妆品注册人、备案人、受托生产企业连续停产1年以上,重新生产前,应当进行全面自查,确认符合要求的。
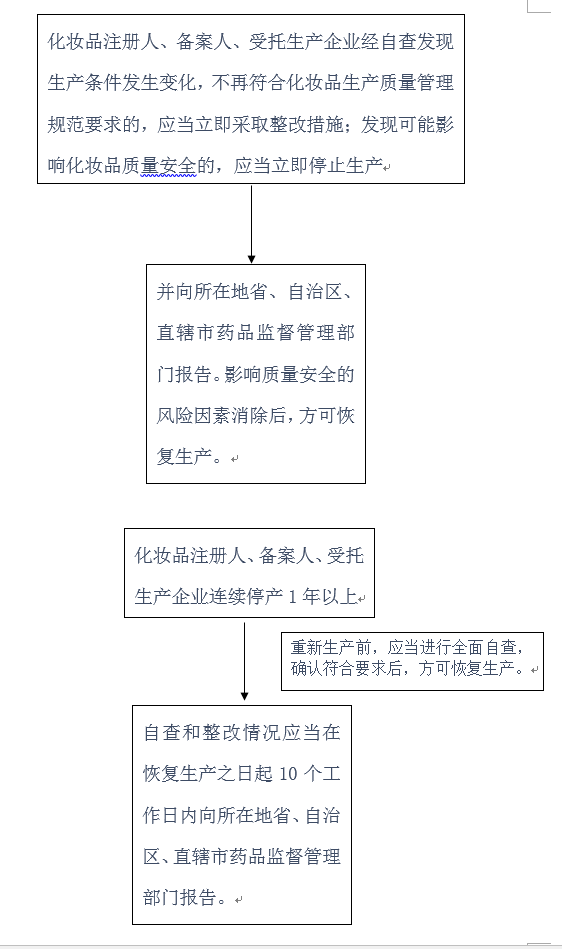
办理流程
流程文字说明
经自查发现生产条件发生变化,不再符合化妆品生产质量管理规范要求的,化妆品注册人、备案人、受托生产企业应当立即采取整改措施;发现可能影响化妆品质量安全的,应当立即停止生产,并向所在地省、自治区、直辖市药品监督管理部门报告。影响质量安全的风险因素消除后,方可恢复生产。省、自治区、直辖市药品监督管理部门可以根据实际情况组织现场检查。
第三十四条 化妆品注册人、备案人、受托生产企业连续停产1年以上,重新生产前,应当进行全面自查,确认符合要求后,方可恢复生产。自查和整改情况应当在恢复生产之日起10个工作日内向所在地省、自治区、直辖市药品监督管理部门报告。
常见问题
问题1:化妆品生产企业停产多久以上,重新生产前,应当进行全面自查?
答:经自查发现生产条件发生变化,不再符合化妆品生产质量管理规范要求的,化妆品注册人、备案人、受托生产企业应当立即采取整改措施;发现可能影响化妆品质量安全的,应当立即停止生产,并向所在地省、自治区、直辖市药品监督管理部门报告。影响质量安全的风险因素消除后,方可恢复生产。省、自治区、直辖市药品监督管理部门可以根据实际情况组织现场检查。
第三十四条 化妆品注册人、备案人、受托生产企业连续停产1年以上,重新生产前,应当进行全面自查,确认符合要求后,方可恢复生产。自查和整改情况应当在恢复生产之日起10个工作日内向所在地省、自治区、直辖市药品监督管理部门报告。
本办事指南摘自药监局官网,如有变动,以官方发布为准。