基本信息
1、办理部门:陕西省药品监督管理局
2、办理方式:网上办理
3、办理地点:陕西省西安市雁塔区丈八沟街道 科技五路21号陕西省食品药品检验研究院院内向西100米(办理窗口:药品生产监管处)
4、咨询电话:029-62288034 CIO咨询:400-003-0818
受理条件
申请事项属于本行政机关职权范围,申请材料齐全、符合法定形式,达到申请条件。
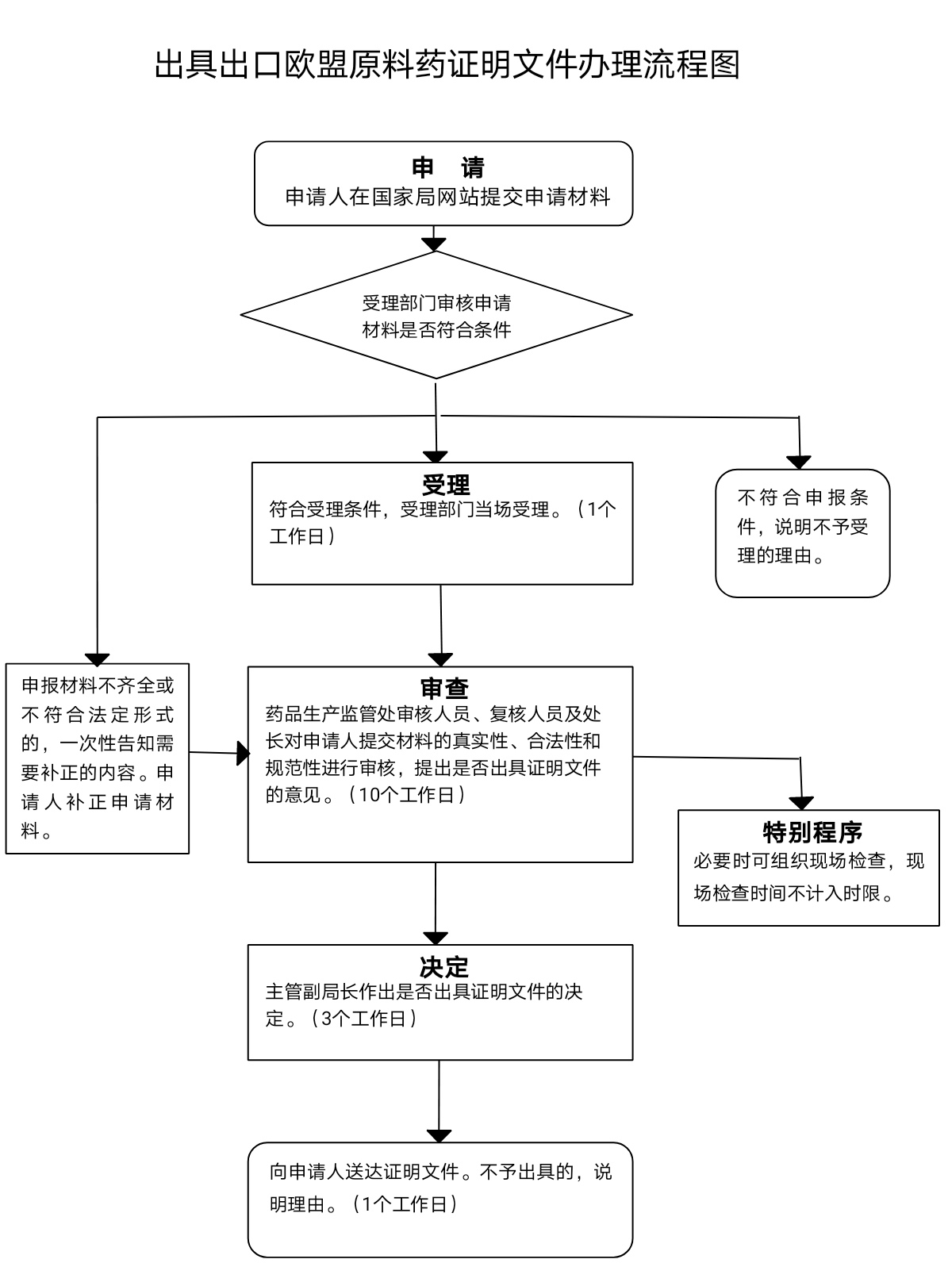
办理流程
流程文字说明
法定办理时限:20个工作日;承诺办理时限:15个工作日
1、受理(时限:1个工作日)
2、审查(时限:10个工作日)
3、决定(时限:3个工作日)
4、送达(时限:1个工作日)
申请材料
1、出口欧盟原料药证明文件申请书;
2、药品生产许可证;
3、营业执照;
4、药品GMP证书;
5、销售合同;
6、药品批准证明文件;
7、药品GMP证书或药品GMP符合性检查结果通知书;
8、检查报告;
9、申报材料的真实性保证声明;
10、委托人授权委托书。
结果样本

常见问题
问题1:该事项的设定依据是什么?
答:国家食品药品监督管理总局关于出口欧盟原料药证明文件有关事项的通知(食药监〔2013〕10号)
各省、自治区、直辖市食品药品监督管理局(药品监督管理局):
2011年6月欧盟发布了原料药新指令2011/62/EU,要求对进口到欧盟成员国的原料药,自2013年7月2日起,其生产企业必须取得出口国药品监管机构签发的证明文件。总局对该指令予以高度关注,通过多种途径与欧盟有关方面进行了沟通协商,研究确定了证明文件出具方式和格式。经征求商务部意见并报国务院同意,现将有关事项通知如下:
一、认真负责地做好证明文件的出具工作
出口欧盟原料药证明文件由原料药生产企业所在地省级食品药品监督管理部门负责出具。为欧盟出具原料药证明文件,既是加强国际合作,参与国际竞争的需要,也为我国加强原料药监管提供了机遇。各省级食品药品监督管理部门要对该项工作予以高度重视,建立健全相关工作制度,制定工作程序,明确工作要求,指定专门处室和人员负责,认真负责地做好出证工作,并为今后加强原料药监管积累数据和经验。具体工作人员要熟悉药品GMP监管工作并具有一定的英语基础。请各省级食品药品监督管理部门将相关联系人信息按附件1要求于2013年5月20日前传真给总局。
本办事指南摘自药监局官网,如有变动,以官方发布为准。
























