 E邀专家
E邀专家
和我们百姓日常生活息息相关的各种食品、化妆品,如今已是琳琅满目,可谓百花齐放。尤其是产品的包装,更是令人眼花缭乱。包装不仅具有保护商品、便于储运、利于计算等基本功能,而且还可以美化商品、引导消费、提高商品附加值。但一些生产厂家违背经济实惠、安全卫生、环保节能的包装规则,为追求促销和高额利润而对商品进行过度包装。商品过度包装一方面浪费自然资源,催生了商品价格虚高,另一方面又制造大量垃圾,对环境造成污染。
很多企业对商品的过度包装不重视,甚至对标准的执行也缺乏认知。我国早在2009年就首次制定了《限制商品过度包装要求 食品和化妆品》强制性国家标准。2021年8月,国家市场监督管理总局、国家标准化管理委员会联合发布了新修订的GB 23350—2021《限制商品过度包装要求 食品和化妆品》(以下简称“标准”)。“标准”将于2023年9月1日正式实施。

违法最高处十万元罚款
1、《固体废物污染环境防治法》第六十八条第二款规定:生产经营者应当遵守限制商品过度包装的强制性标准,避免过度包装。县级以上地方人民政府市场监督管理部门和有关部门应当按照各自职责,加强对过度包装的监督管理。
2、第一百零五条规定:“违反本法规定,生产经营者未遵守限制商品过度包装的强制性标准的,由县级以上地方人民政府市场监督管理部门或者有关部门责令改正;拒不改正的,处二千元以上二万元以下的罚款;情节严重的,处二万元以上十万元以下的罚款。
如何避免过度包装?
笔者通过和一些企业的同行了解得知,“标准”的出台并没有像其他法规一样,得到应有的高度重视,地方监管部门也鲜见组织培训这方面的要求。生产企业在设计包装时仍然我行我素。因此,笔者想通过本篇给大家梳理一下过度包装的要点,希望对你有所警示和帮助。
●“标准”适用于食品和化妆品销售包装,不适用于赠品或非卖品。涉及食品31类、化妆品16类。
●“过度包装”是指超出了商品保护、展示、储存、运输等正常功能要求的包装,主要表现为包装层数过多、包装空隙过大、包装成本过高、选材用料不当等。下边我们逐一解释。
1、包装层数要求:化妆品包装不应超过四层

2、包装空隙率要求:根据净含量计算

包装空隙率计算公式:
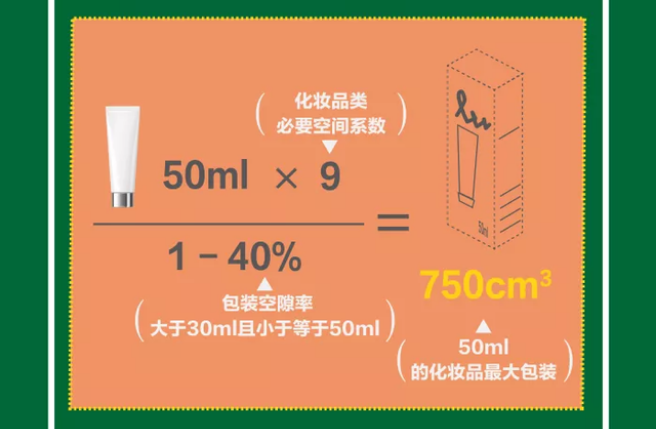
3、包装成本要求:不超过销售价格的20%

加强商品过度包装治理!月饼、粽子、茶叶、保健食品、化妆品注意……
近日,国务院办公厅发布《关于进一步加强商品过度包装治理的通知》,要求强化商品过度包装全链条治理。到2025年,基本形成商品过度包装全链条治理体系,相关法律法规更加健全,标准体系更加完善,行业管理水平明显提升,线上线下一体化执法监督机制有效运行,商品过度包装治理能力显著增强。
通知释放如下信号:
1、高度重视商品过度包装治理工作,坚决遏制商品过度包装现象,为促进生产生活方式绿色转型、加强生态文明建设提供有力支撑。
2、强化商品过度包装全链条治理,加强包装领域技术创新,防范商品生产环节过度包装,避免销售过度包装商品,推进商品交付环节包装减量化,加强包装废弃物回收和处置。
3、加大监管执法力度,加强行业管理,强化执法监督。针对重要节令、重点行业和重要生产经营企业,聚焦月饼、粽子、茶叶、保健食品、化妆品等重点商品。明确依法严格查处生产、销售过度包装商品等违法行为。
对生产源头,《通知》明确督促指导商品生产者严格按照限制商品过度包装强制性标准生产商品,引导商品生产者使用简约包装,优化商品包装设计,减少商品包装层数、材料、成本。
对销售终端,《通知》提出督促指导商品销售者细化采购、销售环节限制商品过度包装有关要求,明确不销售违反限制商品过度包装强制性标准的商品,加强对电商企业的督促指导,鼓励商品销售者向供应方提出有关商品绿色包装和简约包装要求。
综上所述,针对我们化妆品生产企业来说,迫在眉睫的工作是认识到商品过度包装的法规要求和它的重要性,别抱着侥幸的心理,在设计包装的初期就按照国家标准和相关法规要求执行,避免将来造成不必要的资源浪费和经济损失。
如果您正在进行化妆品注册,对包装设计和文案的法规要求不清楚,有可能导致注册申请被拒。CIO合规保证组织帮助客户审核化妆品包装及文案,确保注册顺利通过。点击下方联系我们。
相关文件下载、服务及学习课程:
合规培训:化妆品注册备案必备专题培训
合规服务:化妆品注册——包装文案的撰写或审核
联系专家,获取专家指导意见:e邀专家
 E邀专家
E邀专家
最新推荐

药械企业法律风险预防与应对闭门会

执业药师继教服务

合规破局与价值重塑 医药营销转型实战训练营

药物警戒第三方委托服务

医药企业涉刑防范与应对

生死红线——「医改+反腐」背景下的医药企业生存逻辑与增长路径企业内训

药品医疗器械企业安全风险排查服务

【医药传播】药企品牌 / 产品宣传片制作

医疗器械注册/备案、变更

药品(国产/进口)注册、变更

药品经营许可申请 / 变更

化妆品生产许可申请/变更

医疗器械生产许可申请/变更

药品上市许可持有人的B证申请

药品生产许可申请 / 变更(药厂筹建)

原辅包注册/登记

化妆品注册/备案、变更

药械企业法律风险预防与应对闭门会

执业药师继教服务

合规破局与价值重塑 医药营销转型实战训练营

药物警戒第三方委托服务

医药企业涉刑防范与应对

生死红线——「医改+反腐」背景下的医药企业生存逻辑与增长路径企业内训







