 E邀专家
E邀专家
自从新版GMP要求做“质量回顾”以来,各种统计分析工具与方法逐步被大家所熟知和使用,这是好事,学习之初大都是从模仿开始的,先大胆的用起来,才能慢慢精进,统计的工具也是如此。
而目前在质量回顾中,大家使用的比较普遍的是控制图和过程能力指数,几乎每份回顾中都会或多或少涉及,对于控制图的误用问题,之前已有“GMP对于产品回顾的要求——谈控制图存在的问题及解决方案”做了简单的介绍,今天我们继续来聊聊控制图的难兄难弟“过程能力指数”,这位老弟也是一个坑连坑的坑王。
之前我们聊过它的第一个坑,尤其在使用minitab这些软件时,过程能力指数一键生成,并不设置必须达到然后才可以计算,否则不能计算的前提条件。例如C系列的过程能力指数(Cp\Cpk),要求数据测量准确(MSA)、独立、正态且过程稳定这4个前提条件达到后,才可以计算;而P系列的过程能力指数(Pp\Ppk),则不需要正态和过程稳定的前提即可计算,但有一得就有一失,这样的(Pp\Ppk),只能用于本次分析的数据批,而不外推其它批次;这是第一个坑。
而C系列(Cp\Cpk)和P系列(Pp\Ppk)的过程能力指数之间是什么关系,它们又该怎么称呼?是最大的一个坑,坊间流传最多的是“Cp\Cpk”是短期过程能力指数,而“Pp\Ppk”是长期过程能力指数;那么,有好事者就问了:“多短算是短期?”“多长算是长期?”,有专家说:“通常1个月算短期,半年算是长期”,好事者马上追问那么29天算不算短期?3个月算不算长期?如果你说也差不多吧,那么,28天、27天呢?3个月少一天、少二天……算不算呢?也许你会说不要抬杠嘛,你个杠精!但在澄清事实方面我们需要杠精,就如当年芝诺的“阿喀琉斯跑不过乌龟”悖论一样,这样抬杠般的执着催生了微积分的发明。
那么回过头来想想,是不是所谓长期和短期的提法,本身就有些不妥呢?让我们来看看,经常使用的minitab软件中是怎么写的?如下图所示:
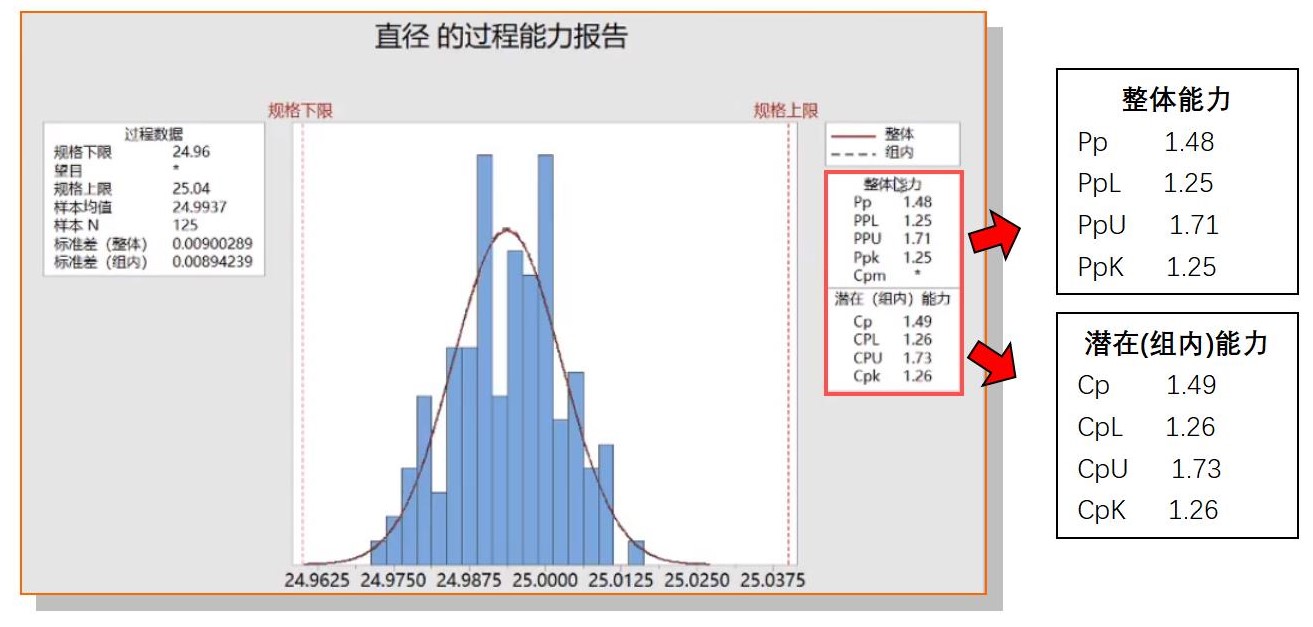
我们看到minitab 是将P系列称为“整体能力”,将C系列称为“潜在或组内能力”(并没有什么“长短期”之分);“整体和潜在”这个叫法中庸一些,它基本上是以能力指数的计算公式为依据来称呼的,严格的来说不能说是对或是错,那我们先来看看它们的计算公式是什么样,有何不同:

从上面的计算公式我们可以看到C系列和P系列,它们从计算的角度看,唯一的区别在于对于标准差的估计方法不同,一个是以“组内变异”进行估算的,而另一个是以“整体变异”来估算的;从这个角度看minitab的“组内”和“整体”的称呼是基本恰当的;但如前面所说的,minitab在计算能力时,一键生成,而不设置一些必备的前提条件,当前提条件达不到时,则不能计算;这样就造成现在业内在计算能力指数时,一键生成简单粗暴,并不管前提条件是否达成。
汇总一下, C系列和P系列能力指数计算的前提条件如下:
Cp\Cpk:1.MSA(测量系统)满足要求;2.数据独立;3.过程稳定;4.数据正态
Pp\Ppk:1. MSA(测量系统)满足要求;2.数据独立
有时候统计比较难学,也和一些统计名称混乱有一定的关系,同一个概念因为翻译或理解的不同,名称是五花八门的,让初学者摸不着北,笔者粗略地汇总了一下C系列和P系列能力指数的不同叫法,如下表:
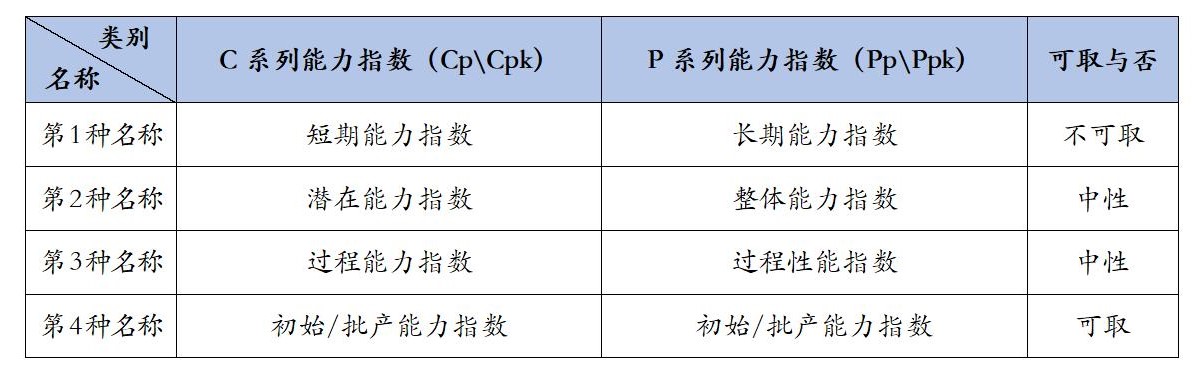
我们换个角度和思路,抛开长期或短期的纠结,以产品批是否为商业化市售产品为分界;在首次验证时的验证批阶段,数据满足Cp\Cpk的4个前提条件我们就计算Cp\Cpk,只满足计算Pp\Ppk的2个前提我们就计算Pp\Ppk;这个首次验证阶段得到的能力指数,我们称之为【初始能力指数】;当它们达到一定的要求后(例如:初始能力指数:要求达到1.67,即SOP生效之前要求,门槛要求),进入产品的商业化批产阶段,那么我们评价【批产能力指数】如批产时数据满足计算Cp\Cpk的4个前提条件我们就计算Cp\Cpk,只满足计算Pp\Ppk的2个前提我们就计算Pp\Ppk。
当然,这里要强调一点,满足4个前提条件计算的Cp\Cpk,是可以进行外推,可以对其它批次进行统计推断的,推断预估其它批次的质量状况;而只满足2个前提条件计算的Pp\Ppk,只能对本批进行判断且结果仅供参考,不能进行外推,进行任何统计推断的。
综上,从制造业产品的全生命周期以预防为主、强调全流程过程管理的角度看,对过程能力指数的理解和应用,还是以验证阶段的“初始能力指数”和商业化生产阶段的“批产能力指数”来实操和应用更加合理。
相关文件下载、服务及学习课程:
合规培训:限免-药品生产现场管理培训
合规服务:质量风险评估
联系专家,获取专家指导意见:e邀专家
 E邀专家
E邀专家
最新推荐
热门观点

药械企业法律风险预防与应对闭门会

执业药师继教服务

合规破局与价值重塑 医药营销转型实战训练营

药物警戒第三方委托服务

医药企业涉刑防范与应对

生死红线——「医改+反腐」背景下的医药企业生存逻辑与增长路径企业内训

药品医疗器械企业安全风险排查服务

【医药传播】药企品牌 / 产品宣传片制作

医疗器械注册/备案、变更

药品(国产/进口)注册、变更

药品经营许可申请 / 变更

化妆品生产许可申请/变更

医疗器械生产许可申请/变更

药品上市许可持有人的B证申请

药品生产许可申请 / 变更(药厂筹建)

原辅包注册/登记

化妆品注册/备案、变更

药械企业法律风险预防与应对闭门会

执业药师继教服务

合规破局与价值重塑 医药营销转型实战训练营

药物警戒第三方委托服务

医药企业涉刑防范与应对

生死红线——「医改+反腐」背景下的医药企业生存逻辑与增长路径企业内训







