 E邀专家
E邀专家
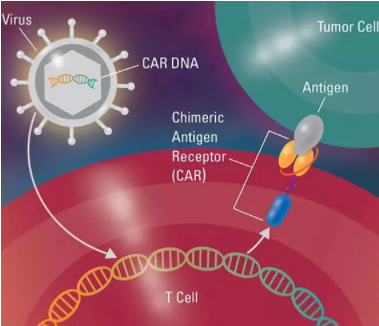
120万一针的抗癌药可谓是让干细胞治疗产品进入大众视野。患有弥漫大B细胞淋巴瘤的上海陈阿姨在采用阿基仑赛注射液治疗两个月后,发现体内暂时没有癌细胞,症状完全得到了缓解,于是从上海瑞金医院出院。这是国内首例CAR-T治疗的淋巴瘤患者出院案例。一时之间,癌症有了治愈的可能引起社会的广泛关注,CAR-T细胞疗法成了最火热的领域。
随之而来的,是国家监管政策的不断完善和加强。我国对干细胞技术一直非常重视,在上世纪90年代初就制定了《人的体细胞治疗及基因治疗临床研究质控要点》等一系列规范文件来促进干细胞研究及临床产业的发展。2015 年之后,我国在政策上加大支持力度,从规范监管、技术支持以及资金三个方面促进行业的发展。
今年8月17日,国家药监局药审中心发布了关于《人源性干细胞产品药学研究与评价技术指导原则》的征求意见稿。针对干细胞治疗产品出台的针对性药学、药理毒理和临床研究方面做了比较细致的指导原则,进一步规范和指导人源性干细胞产品的药学研发和申报,促进干细胞产业的合规发展。
这个征求意见稿明确了哪几类干细胞可以按照国家药监局的监管进行申报,包括人源性的成体干细胞(其中的代表就是现在被最广泛研究的各种来源的间充质干细胞)、人胚干细胞和诱导性多能干细胞扩增、诱导分化,或成熟体细胞转(分)化获得的干细胞及衍生细胞。明确了可申报的范围,这对研究者、从业人员、投资机构而言,是一个很重要的政策信号。此外,征求意见稿不仅明确可以申请药物的单纯的细胞类型,还前瞻性地指明组织工程复合材料也在可申报范围内。针对目前困扰生产企业最核心的干细胞来源问题,指导原则也明确了企业可以和国家设立的干细胞库合作,对接国家人类遗传中心。
与此同时,我们也感受到,征求意见稿更加明确了干细胞的产业化路径,强调了GMP的要求。那么,CIO合规保证组织小编建议,投资者在考查干细胞药物企业时,要重点关注其GMP建厂能力,或者关注一些有细胞领域GMP经验的第三方服务机构,通过第三方的合规指导,共同推进GMP质量管理体系合规建设。当然在这个过程当中,需要与监管当局进行充分的沟通,充分理解指导原则的精髓。CIO合规保证组织,目前在细胞领域GMP建厂方面积累了一定的经验,欢迎广大投资者、从业者联系咨询,为即将到来的人源性干细胞研究和商业化黄金发展期做足准备。
相关文件下载、服务及学习课程:
合规文库:《人源性干细胞产品药学研究与评价技术指导原则》(征求意见稿)
合规培训:微生物基础知识培训
合规服务:GMP合规审计(符合性检查)
联系专家,获取专家指导意见:e邀专家
 E邀专家
E邀专家
最新推荐
热门观点

药械企业法律风险预防与应对闭门会

执业药师继教服务

合规破局与价值重塑 医药营销转型实战训练营

药物警戒第三方委托服务

医药企业涉刑防范与应对

生死红线——「医改+反腐」背景下的医药企业生存逻辑与增长路径企业内训

药品医疗器械企业安全风险排查服务

【医药传播】药企品牌 / 产品宣传片制作

医疗器械注册/备案、变更

药品(国产/进口)注册、变更

药品经营许可申请 / 变更

化妆品生产许可申请/变更

医疗器械生产许可申请/变更

药品上市许可持有人的B证申请

药品生产许可申请 / 变更(药厂筹建)

原辅包注册/登记

化妆品注册/备案、变更

药械企业法律风险预防与应对闭门会

执业药师继教服务

合规破局与价值重塑 医药营销转型实战训练营

药物警戒第三方委托服务

医药企业涉刑防范与应对

生死红线——「医改+反腐」背景下的医药企业生存逻辑与增长路径企业内训






