 E邀专家
E邀专家
国家药监局7月31日发布《优化创新药临床试验审评审批试点工作方案》,拟通过一年时间的试点,在试点区域(省域)、试点(临床)机构,对试点项目临床试验申请的审评审批进行优化改革,实现30个工作日内完成创新药临床试验申请的审评审批,缩短药物临床试验启动的用时。
相对于目前60个工作日的默示许可,本次试点,审评审批时间有望缩短一半!
这无疑又是国家药监局持续深化药品审评审批制度改革,提升药品审评审批效能,支持创新药研发的又一个重磅作为!
2017年10月份,中共中央办公厅、国务院办公厅印发《关于深化审评审批制度改革鼓励药品医疗器械创新的意见》以来,国家药监局持续作为,通过多种优化改革鼓励创新药的研发,对企业而言,这都是热情鼓励的火焰!
然而,在市场这一面,对创新药的研发投入却是浇来冷冷的海水!
近几年来,由于国家医保控费,药品带量集采等的洗礼,创新药的盈利预期也受到前所未有的挑战,资本投资创新药的热情骤减。
以创新药研发投入为典型特征的恒瑞制药为例,“CIO在线”查询该企业近5年来研发投入、企业利润、企业市值等公开数据,发现从2020年开始,该企业的研发投入开始持平、没有新增,而企业市值却有明显下降,这就是市场对创新药研发投入的真实反馈。
恒瑞制药近5年研发投入
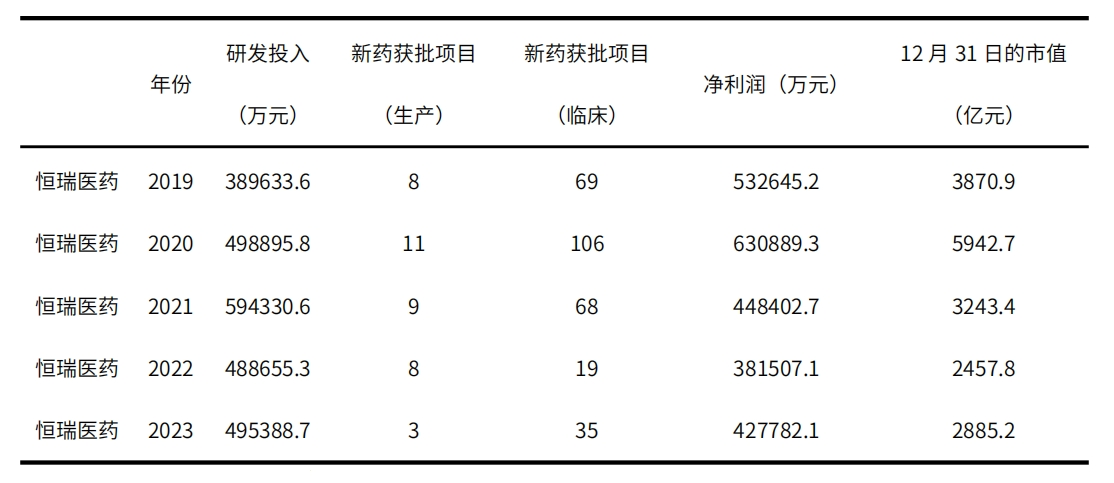
数据来源:上市公司年报
一边是火焰,一边是海水。
创新药的发展既有机遇更有挑战!
CIO合规保证组织可为您提供药品注册申请、注册现场核查服务,欢迎点击下方链接,提交您的需求!
相关文件下载、服务及学习课程:
合规文库:药品注册管理办法(2020年)
合规培训:药品注册现场核查要点及判定原则
委托定制:药品注册申请
联系专家,获取专家指导意见:e邀专家
*以上文章仅代表作者个人观点。
有疑问、问专家
提问
 E邀专家
E邀专家
最新推荐
热门观点

药械企业法律风险预防与应对闭门会

执业药师继教服务

合规破局与价值重塑 医药营销转型实战训练营

药物警戒第三方委托服务

医药企业涉刑防范与应对

生死红线——「医改+反腐」背景下的医药企业生存逻辑与增长路径企业内训

药品医疗器械企业安全风险排查服务

【医药传播】药企品牌 / 产品宣传片制作

医疗器械注册/备案、变更

药品(国产/进口)注册、变更

药品经营许可申请 / 变更

化妆品生产许可申请/变更

医疗器械生产许可申请/变更

药品上市许可持有人的B证申请

药品生产许可申请 / 变更(药厂筹建)

原辅包注册/登记

化妆品注册/备案、变更

药械企业法律风险预防与应对闭门会

执业药师继教服务

合规破局与价值重塑 医药营销转型实战训练营

药物警戒第三方委托服务

医药企业涉刑防范与应对

生死红线——「医改+反腐」背景下的医药企业生存逻辑与增长路径企业内训
分享






