基本信息
1、办理部门:陕西省药品监督管理局
2、办理方式:窗口办理、网上办理、快递申请
3、办理地点:陕西省西安市雁塔区 科技五路21号陕西省食品药品检验研究院院内向西100米(办理窗口:综合窗口)
4、咨询电话:029-62288101、029-62288254 CIO咨询:400-003-0818
受理条件
申请事项属于本行政机关职权范围,申请材料齐全、符合法定形式,达到申请条件。
办理流程
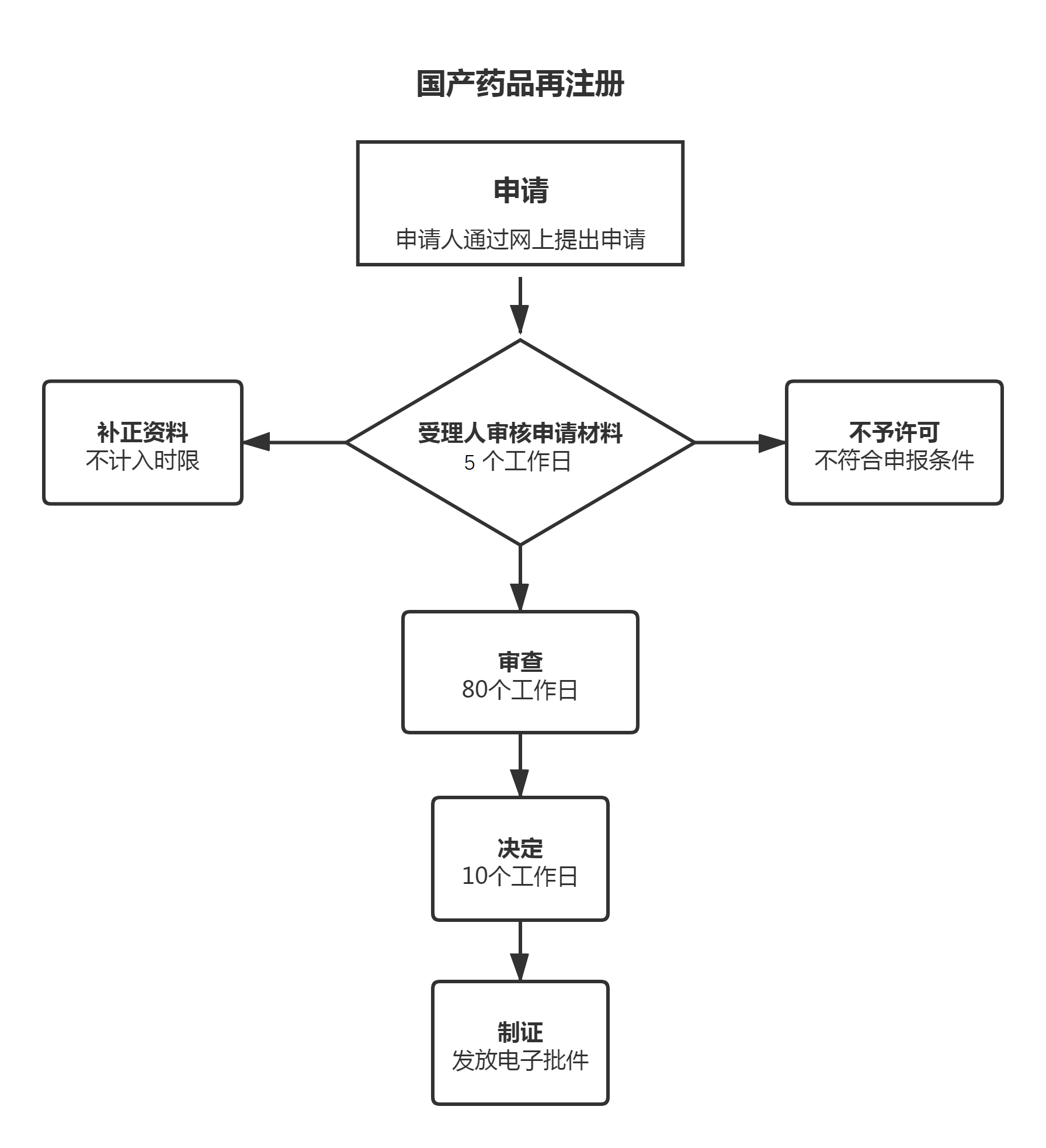
流程文字说明
法定办理时限:120个工作日;承诺办理时限:90个工作日
1、受理(时限:5个工作日)
2、审查(时限:80个工作日)
3、决定(时限:10个工作日)
4、制证(时限:0个工作日)
申请材料
1、真实性承诺书;
2、药品批准证明文件;
3、药品再注册申请表;
4、药品生产企业对再注册药品的安全性、有效性和质量可控性的综合评价报告;
5、药品生产许可证;
6、五年内药品临床使用情况及不良反应情况总结;
7、药品GMP符合性检查结果通知书;
8、五年内生产、销售、抽验情况总结;
9、药品说明书;
10、药品质量标准;
11、药品标签;
12、药品批准证明文件有关要求完成情况;
13、药品处方、生产工艺、药品标准;
14、生产药品制剂所用原料药的来源;
15、上一年度企业年度报告。
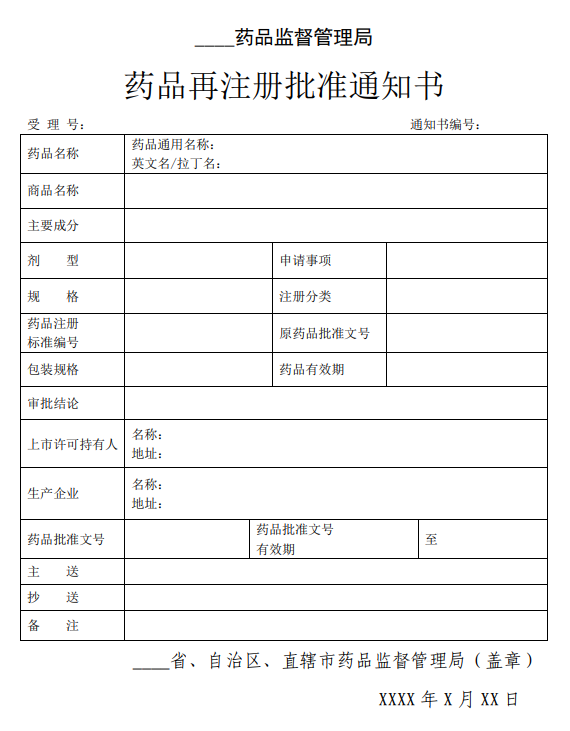
结果样本
常见问题
问题1:该事项的设定依据是什么?
答:《中华人民共和国药品管理法实施条例》(2002年8月4日国务院令第360号,2016年2月6日予以修改)
第四十一条 ……药品批准文号的再注册由省、自治区、直辖市人民政府药品监督管理部门审批,并报国务院药品监督管理部门备案;《进口药品注册证》、《医药产品注册证》的再注册由国务院药品监督管理部门审批。
《药品注册管理办法》
第六条 省、自治区、直辖市药品监督管理部门负责本行政区域内以下药品注册相关管理工作:
(一)境内生产药品再注册申请的受理、审查和审批;
第十二条 药品注册证书有效期为五年,药品注册证书有效期内持有人应当持续保证上市药品的安全性、有效性和质量可控性,并在有效期届满前六个月申请药品再注册。
第八十二条 持有人应当在药品注册证书有效期届满前六个月申请再注册。境内生产药品再注册申请由持有人向其所在地省、自治区、直辖市药品监督管理部门提出,境外生产药品再注册申请由持有人向药品审评中心提出。
本办事指南摘自药监局官网,如有变动,以官方发布为准。
























