 E邀专家
E邀专家
氯倍他索丙酸脂、本维莫德、他克莫司、赛庚啶……这些物质或为激素,或为某些疾病治疗用药物,却在化妆品中被检测了出来,这一事实让广大消费者内心一惊。我们日常接触到、使用的化妆品到底安全吗?
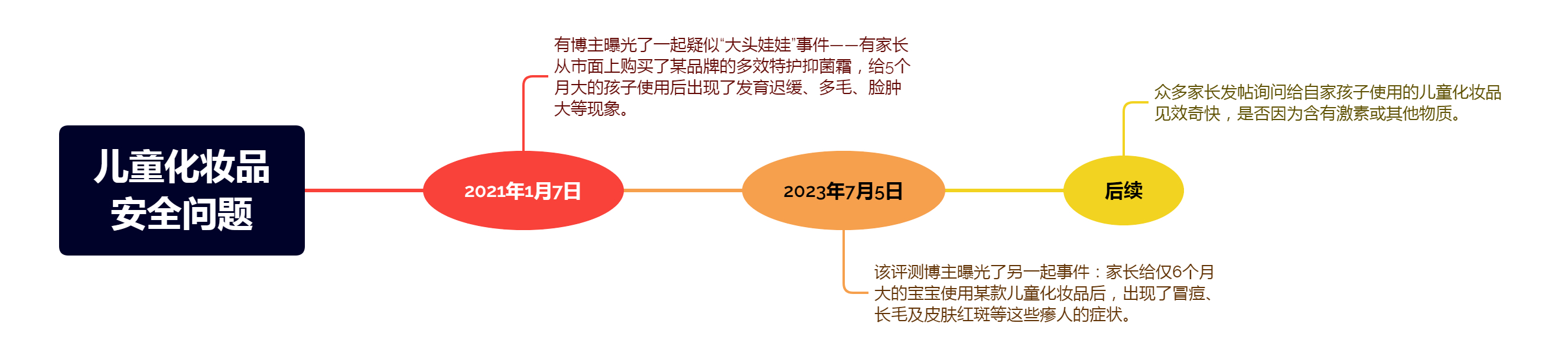
博主曝光儿童化妆品安全问题
可供儿童使用的化妆品尚且能检测出各种激素、违禁添加物质,更何况普通化妆品呢?从这几起事件以及广大网友的评论来看,化妆品的安全质量问题值得进一步查验。
依据《化妆品监督管理条例》第三十条规定,化妆品原料、直接接触化妆品的包装材料应当符合强制性国家标准、技术规范。不得使用超过使用期限、废弃、回收的化妆品或者化妆品原料生产化妆品。同时,在《化妆品安全技术规范》(2015年版)以及后续更新的《化妆品禁用原料目录》中,就已将抗组胺药、抗感染类药物(包括但不限于抗生素类)、激素类物质列入了化妆品禁用组分。前面提到的企业并未遵守相关规定,违禁添加物质,危害到了使用者的身体健康。
针对公众使用化妆品时的安全问题,国家药监局化妆品监管司于2023年6月21日召开了化妆品“一号多用”违法行为专项检查动员部署会。该会议确定了本次专项行动的重点,即集中排查和治理化妆品“一号多用”的违法行为,这些行为包括在产品标签上违法标注除了化妆品注册备案资料以外的文字、商标、标识,或者通过其他方式套用特殊化妆品注册证编号或普通化妆品备案编号。检查将主要关注以下三种情形:
一、“一号多名称”形式套用化妆品注册证号、备案编号的情形
通过在产品标签上违法标注已注册或者备案产品的名称以外的其他名称或者易使消费者视为产品名称的文字,导致消费者对该产品的名称产生误解。
在“成分党”大行其道的今天,各大企业常常会因某种成分受到大家追捧就往产品上标注该成分名,更换包材后,成分不变但产品名又发生了变化,这就造成了“一号多名称”现象的泛滥。
二、“一号多商标”形式套用化妆品注册证号、备案编号的情形
通过在产品标签上违法标注化妆品注册备案资料载明的商标以外的其他商标或者易使消费者视为商标的标识,导致消费者对该产品的质量安全责任主体产生误解。
有的企业在产品包装上会加上除了产品名称以外的商标,如本来不是自己公司持证的产品却贴上了自己公司的商标,误导了消费者以为该产品是自己品牌的。
三、“一号多主体”形式套用化妆品注册证号、备案编号的情形
通过在产品标签上违法标注“监制”“出品”“品牌授权人”等相关词语,导致消费者对该产品的质量安全责任主体产生误解。
除了上述的词语,还有的企业会在产品上标注“技术支持”、“联合出品”等等,以此来做品牌背书,容易让消费者误以为产品的质量安全责任主体是标注的单位。
上述问题在各种化妆品中其实都有涉及,具体情况也远不止文中所列举的这些。造成“一号多用”的原因有很多,从原料供应商到产品生产企业,负责管理每个环节的不同人员都会有着自己的考量。但话又说回来了,既然目前各地药监局已经陆续组织开展专项检查了,倘若企业真的在产品上标注了易让人误解的内容,不管是为了大众使用化妆品的安全性着想,还是为了尽最大可能降低企业的损失,能自行整改就尽快整改吧,不然等到接受检查、处罚结果出来之后,再来后悔也没有用了。
相关文件下载、服务及学习课程:
合规文库:《化妆品安全技术规范》(2015年版)
合规培训:化妆品注册备案必备专题培训
委托定制:化妆品注册备案
联系专家,获取专家指导意见:e邀专家
*以上文章仅代表作者个人观点
 E邀专家
E邀专家
最新推荐

药械企业法律风险预防与应对闭门会

执业药师继教服务

合规破局与价值重塑 医药营销转型实战训练营

药物警戒第三方委托服务

医药企业涉刑防范与应对

生死红线——「医改+反腐」背景下的医药企业生存逻辑与增长路径企业内训

药品医疗器械企业安全风险排查服务

【医药传播】药企品牌 / 产品宣传片制作

医疗器械注册/备案、变更

药品(国产/进口)注册、变更

药品经营许可申请 / 变更

化妆品生产许可申请/变更

医疗器械生产许可申请/变更

药品上市许可持有人的B证申请

药品生产许可申请 / 变更(药厂筹建)

原辅包注册/登记

化妆品注册/备案、变更

药械企业法律风险预防与应对闭门会

执业药师继教服务

合规破局与价值重塑 医药营销转型实战训练营

药物警戒第三方委托服务

医药企业涉刑防范与应对

生死红线——「医改+反腐」背景下的医药企业生存逻辑与增长路径企业内训






