 E邀专家
E邀专家
1. 背景介绍
生物大分子(单抗/双抗/ADC)的成品生产工艺包括原液解冻工艺、除菌过滤工艺、灌装工艺、冻干工艺(冻干剂型)等主要步骤。成品生产工艺中操作参数可能会影响到以下关键质量属性CQA:水分含量(冻干剂型)、SEC纯度、无菌、不溶性微粒、微生物限度、吐温含量、蛋白质含量、装量等。
在商业化生产三批工艺验证PV时,已经确定成品生产工艺,在这之前,需要确认生产工艺,就需要对生产工艺操作参数进行工艺表征PC。本文重点介绍除菌过滤工艺的表征研究,主要关系到产品的无菌、SEC纯度、不溶性微粒、吐温含量、蛋白质含量等。
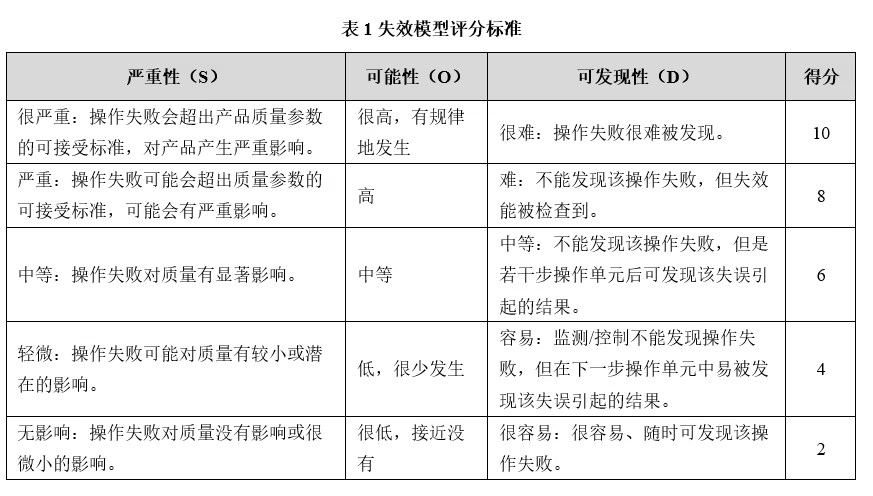
依据除菌过滤工艺影响到的CQA,对工艺参数进行风险评估。风险评估采用失败模型影响分析(FEMA)工具进行分析,失败模型影响分析评分内容包括严重性S(Severity),发生的可能性O(Occurrence)和结果的可发现性D(Defection),根据风险优先指数RPN(RPN=S×O×D),制定表征研究策略。失效模型的评分标准见表1。

2. 除菌过滤工艺表征研究
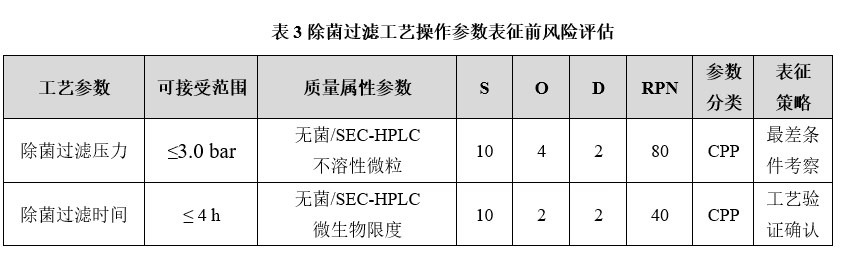
抗体类成品为非最终灭菌的注射剂型,抗体原液需要进行除菌过滤,目的是达到注射剂的无菌要求。除菌过滤工艺的表征主要从过滤膜吸附表征研究、压力表征研究、过滤膜通量表征研究等方面进行考察。
2.1.1 设备与材料
电子天平、恒压过滤容器(1 L压力罐)、过滤膜(0.22 μm孔径 /4.5 cm2膜面积/PES膜材质)
2.1.2 滤膜吸附表征研究
除菌过滤膜材可能对抗体类成品中的蛋白质和吐温产生吸附,吸附导致蛋白质含量和吐温浓度的下降,可能会影响蛋白质的稳定性或者药效,但其它辅料均为小分子物质不易被吸附,容易透过 0.22 μm 的膜。因此商业化生产时,需要确认过滤膜材对蛋白质和吐温的吸附,以确保除菌过滤前后的蛋白质含量和吐温浓度在可接受范围内。
实验室环境下,利用 scale down 缩小模型,使用与的生产时相同材质的除菌过滤膜,膜面积 4.5 cm2的小型过滤膜,模拟成品生产过程中的原液除菌过滤操作。在过滤过程中,使用与生产时相同的过滤压力如 0.15 bar,在不同时间点下取样,考察过滤过程中的蛋白质含量(15.0±1.0 mg/mL)、吐温浓度(0.08±0.04 mg/mL)的质量变化情况。
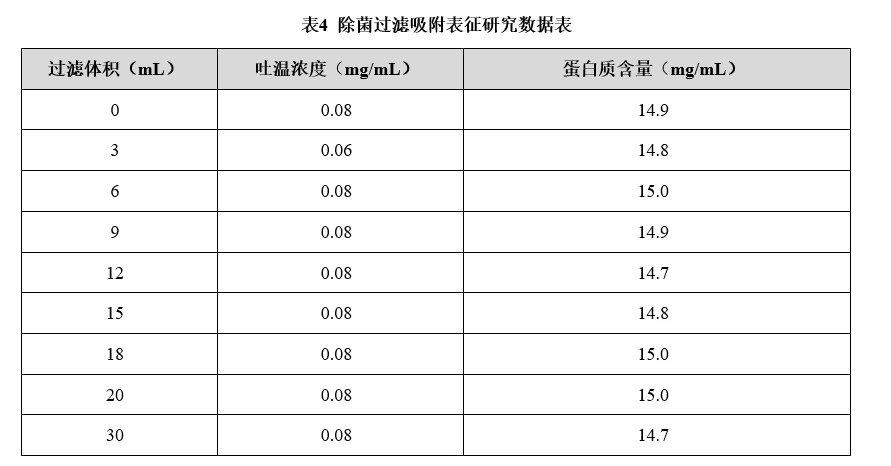

结果表明在过滤过程中,随着过滤体积的增长,小型0.22 μm过滤器(PES膜、4.5 cm2)对蛋白质含量均无吸附影响。在过滤初期,滤膜对吐温有少量吸附,当过滤载量达到1.3 mL/cm2(过滤体积6 mL)时,达到吸附饱和,后期无明显吸附。故在商业化生产除菌过滤时,以过滤膜面积计算需要排空的体积,等滤膜达到饱和吸附后进行灌装,对成品生产中吐温含量无明显影响。
2.1.3 除菌过滤压力表征研究
在除菌过滤中,无论是采用恒压过滤还是恒流过滤,过滤压力越高(流速越快),产生的剪切力越大,对抗体类蛋白纯度稳定性影响越大。采用最差条件方法进行考察,即在最大压力下进行过滤,考察过滤样品的质量指标,确定除菌过滤压力可接受范围。
在实验室环境下,使用与生产所用相同材质的小型过滤膜(0.22μm/ PES膜/4.5 cm2)作为缩小模型,模拟生产过程中的原液过滤操作,分别设定过滤压力3.0 bar、2.0 bar,过滤前后取样考察SEC纯度,暂不考察无菌以及不溶性微粒。
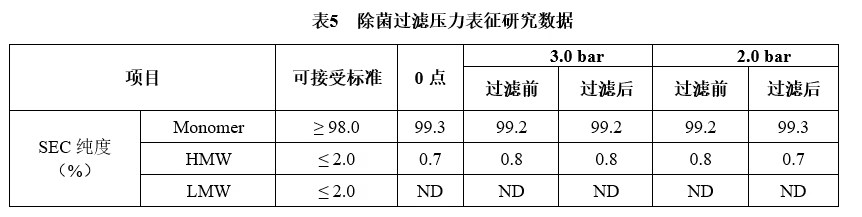
在3.0 bar、2.0 bar过滤压力下,过滤前后SEC-HPLC纯度(聚体、主峰、片段比例)均未显著性有变化,故在生产中的过滤压力可接受范围为≤3.0 bar。
2.1.4 过滤通量表征研究
抗体类蛋白除菌过滤在确定滤膜材质后,需要在scale down模型下,测试除菌过滤器的通量,来满足除菌过滤时间内完成一定体积的除菌过滤操作。采用通用的过滤模型公式:d2t/dV2=k(dt/dV)n,其中t =过滤时间、V =滤过体积、k =常数、n =堵塞模型。
对于符合逐渐堵塞模型的料液,上述公式中n =1。如果以t/V 和t 作图,两者为线性关系,就可以预测长时间过滤后的堵塞情况,故可以对工艺所需要的过滤膜面积进行计算。Vmax技术选型试验:通过恒压过滤试验,将过滤得到的数据拟合计算出Vmax(滤器能处理的最大过滤载量)和滤器的初始过滤通量,计算出工艺时间内处理料液所需的除菌过滤器最小面积,再结合操作安全系数,得到最终的除菌过滤器选型。
对于非堵塞型料液(类似水),在室温下其粘度接近于1 cp,且通常不会堵塞滤膜。可以在同种小型除菌过滤器上通过压力流速实验计算出不同压力下的过滤通量,在保持过滤通量一致的原则下,可线性放大得到最终的除菌过滤器配置。
依据以上设计思路,本次采用与生产同材质同孔径的小型过滤器(缩小模型)来进行一系列实验,摸索抗体类成品商业化生产过程中除菌过滤操作参数范围,为除菌过滤工艺操作参数的设定提供数据支持。
首先进行Vmax实验,在0.15 bar过滤压力下小型过滤膜(0.22μm/ PES膜/4.5 cm2)记录各个时间点下已过滤原液的体积,以t为横坐标,t/v为纵坐标作出该小型滤器的拟合线性回归曲线。曲线需满足相关系数R²>0.99,建立线性回归方程曲线。
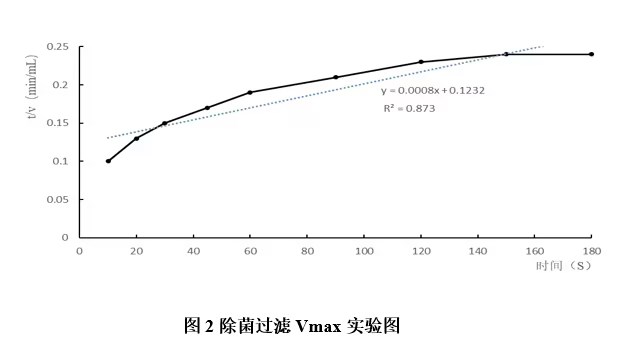
根据除菌过滤Vmax实验数据图可知: Vmax回归曲线R2=0.873<0.99,即t/V和t不存在线性关系,即n≠1,故此料液不属于堵塞性液体过滤物料。
判断出抗体类原液不符合逐渐堵塞模型,接下来进行压力流速曲线实验:在不同压力下将原液通过小型过滤器(缩小模型),并在一定时间间隔(如1 min)记录滤过液体积,计算不同压力下的过滤流速(各个点的平均流速),以流速(mL/min)为横坐标,压力(bar)为纵坐标作出该小型滤器的曲线图,拟合线性回归曲线。曲线需满足相关系数R²>0.99,建立线性回归方程。
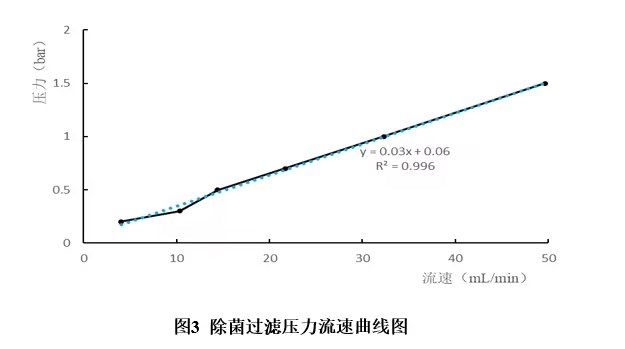
依据过滤压力流速曲线图:回归方程y=0.03x+0.06,其中y代表过滤压力bar,x代表过滤流速mL/min,回归曲线R2=0.9961>0.99,回归方程具有统计学显著意义。在0.2 bar压力下,缩小模型膜面积 4.5 cm2得到的 过滤 通量 约 为 622 L/h/ m2,商业化生产过滤工艺按照过滤通量保持一致的原则,进行scale up放大,除菌过滤工艺要求 2小时内完成 100 L原液的过滤 ,则需要 选择膜面积≥1200 cm2的除菌过滤器(安全系数 1.5)。
CIO合规保证组织,为广大药企提供药品生产合规整体解决方案委托定制服务。点击下方链接,提交您的需求!
相关文件下载、服务及学习课程:
合规培训:工艺验证与工艺设计(上)
联系专家,获取专家指导意见:e邀专家
*以上文章仅代表作者个人观点
 E邀专家
E邀专家
最新推荐
热门观点

药械企业法律风险预防与应对闭门会

执业药师继教服务

合规破局与价值重塑 医药营销转型实战训练营

药物警戒第三方委托服务

医药企业涉刑防范与应对

生死红线——「医改+反腐」背景下的医药企业生存逻辑与增长路径企业内训

药品医疗器械企业安全风险排查服务

【医药传播】药企品牌 / 产品宣传片制作

医疗器械注册/备案、变更

药品(国产/进口)注册、变更

药品经营许可申请 / 变更

化妆品生产许可申请/变更

医疗器械生产许可申请/变更

药品上市许可持有人的B证申请

药品生产许可申请 / 变更(药厂筹建)

原辅包注册/登记

化妆品注册/备案、变更

药械企业法律风险预防与应对闭门会

执业药师继教服务

合规破局与价值重塑 医药营销转型实战训练营

药物警戒第三方委托服务

医药企业涉刑防范与应对

生死红线——「医改+反腐」背景下的医药企业生存逻辑与增长路径企业内训






