化学药品生产场地变更与工艺变更研究与申报
相关推荐:

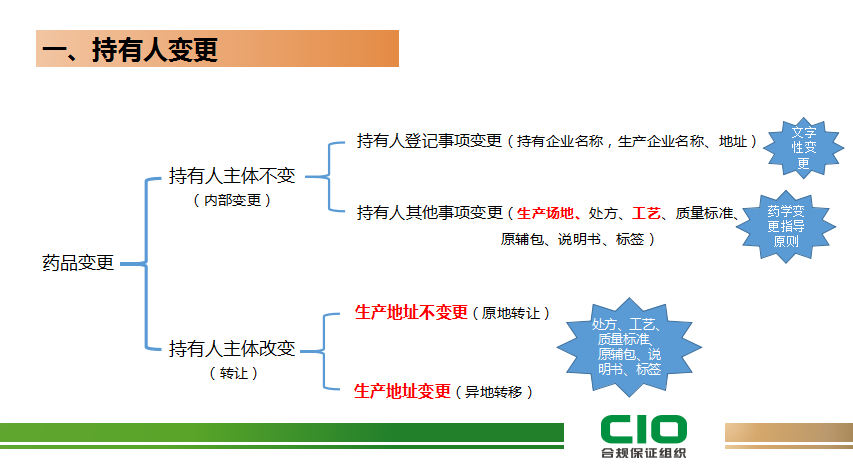
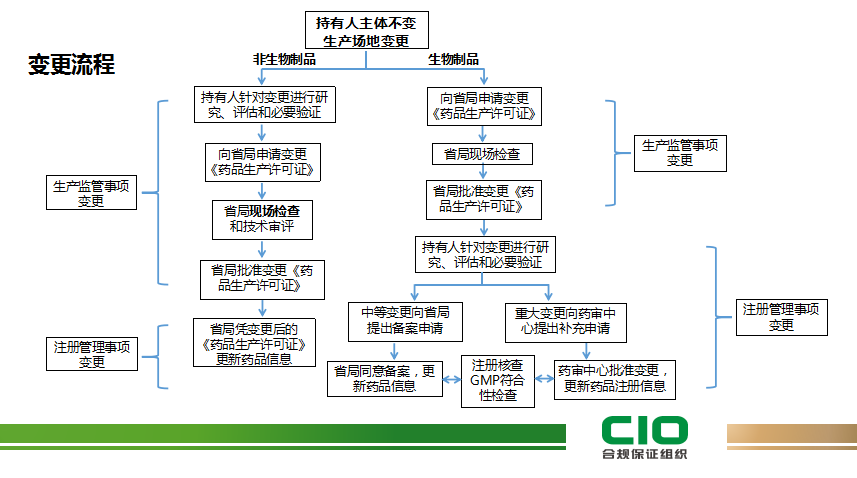
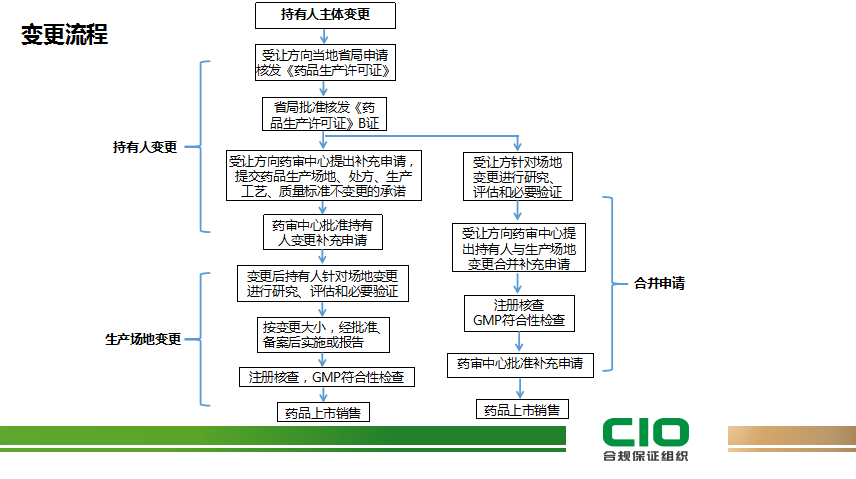
药品上市后变更是药品全生命周期质量管理的重要内容,2021年1月13日,国家药监局发布了《药品上市后变更管理办法(试行)》,进一步明晰了“基于风险的药品变更分类管理原则”,那么持有人变更一般会涉及哪些内容?持有人的变更路径该如何设计?如何去界定重大变更、中等变更和微小变更这三种变更呢?CIO在线帮您详细梳理和讲解。

本课件内含48页,主要从以下4个方面进行展开:
1、持有人变更分类
2、生产地址变更
3、工艺变更
4、变更申报要求
更多拓展内容可观看培训视频《百城行:化学药品生产场地变更与工艺变更研究与申报》。

1、逻辑清晰
课程逻辑清晰,结构完整,构建药品生产质量管理知识体系。
2、远程教学
不受空间限制,充分调动高质量培训资源,大大提高培训效率。
3、行业积淀
讲师有多年药品生产质量管理经验,实践与知识完美结合。

1、可开发票
2、课件售出后,我们将安排专员进行实时跟踪回访,全程为您答疑!
3、若您在购买或使用课件过程中遇到任何问题,亦可点击“在线咨询”联系我们的客服。我们将竭诚为您解答,谢谢!
4、服务咨询热线:400-003-0818

本预览仅为部分内容,查看完整课件,请点击“立即下载”进行购买下载。


药械企业法律风险预防与应对闭门会

执业药师继教服务

合规破局与价值重塑 医药营销转型实战训练营

药物警戒第三方委托服务

医药企业涉刑防范与应对

生死红线——「医改+反腐」背景下的医药企业生存逻辑与增长路径企业内训

药品医疗器械企业安全风险排查服务

【医药传播】药企品牌 / 产品宣传片制作

医疗器械注册/备案、变更

药品(国产/进口)注册、变更

药品经营许可申请 / 变更

化妆品生产许可申请/变更

医疗器械生产许可申请/变更

药品上市许可持有人的B证申请

药品生产许可申请 / 变更(药厂筹建)

原辅包注册/登记

化妆品注册/备案、变更

药械企业法律风险预防与应对闭门会

执业药师继教服务

合规破局与价值重塑 医药营销转型实战训练营

药物警戒第三方委托服务

医药企业涉刑防范与应对

生死红线——「医改+反腐」背景下的医药企业生存逻辑与增长路径企业内训




