 E邀专家
E邀专家
贝朗医疗(上海)国际贸易有限公司对一次性使用中心静脉导管包主动召回(沪药监械主召2024-064)
上海市 阅读 482
收藏
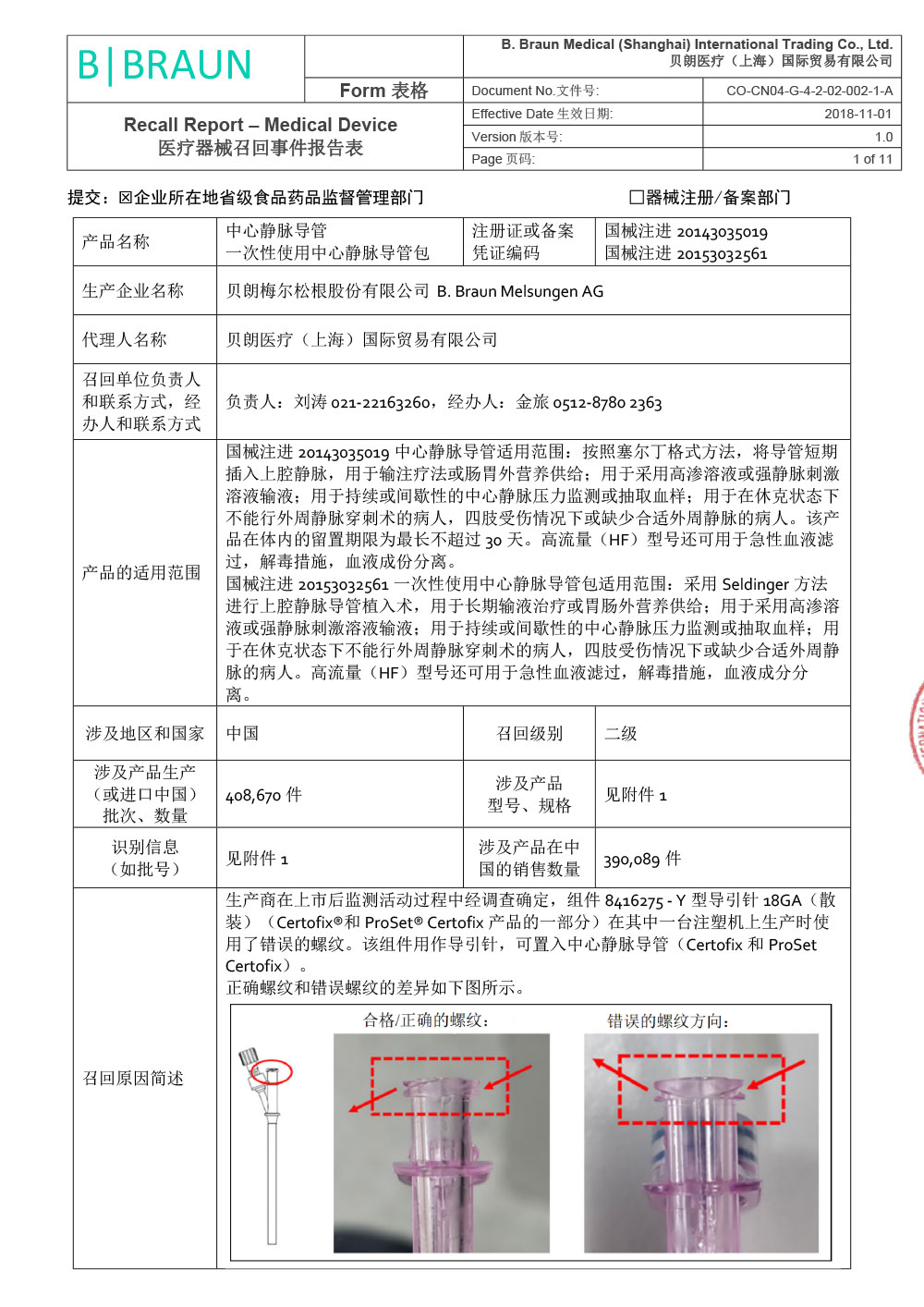
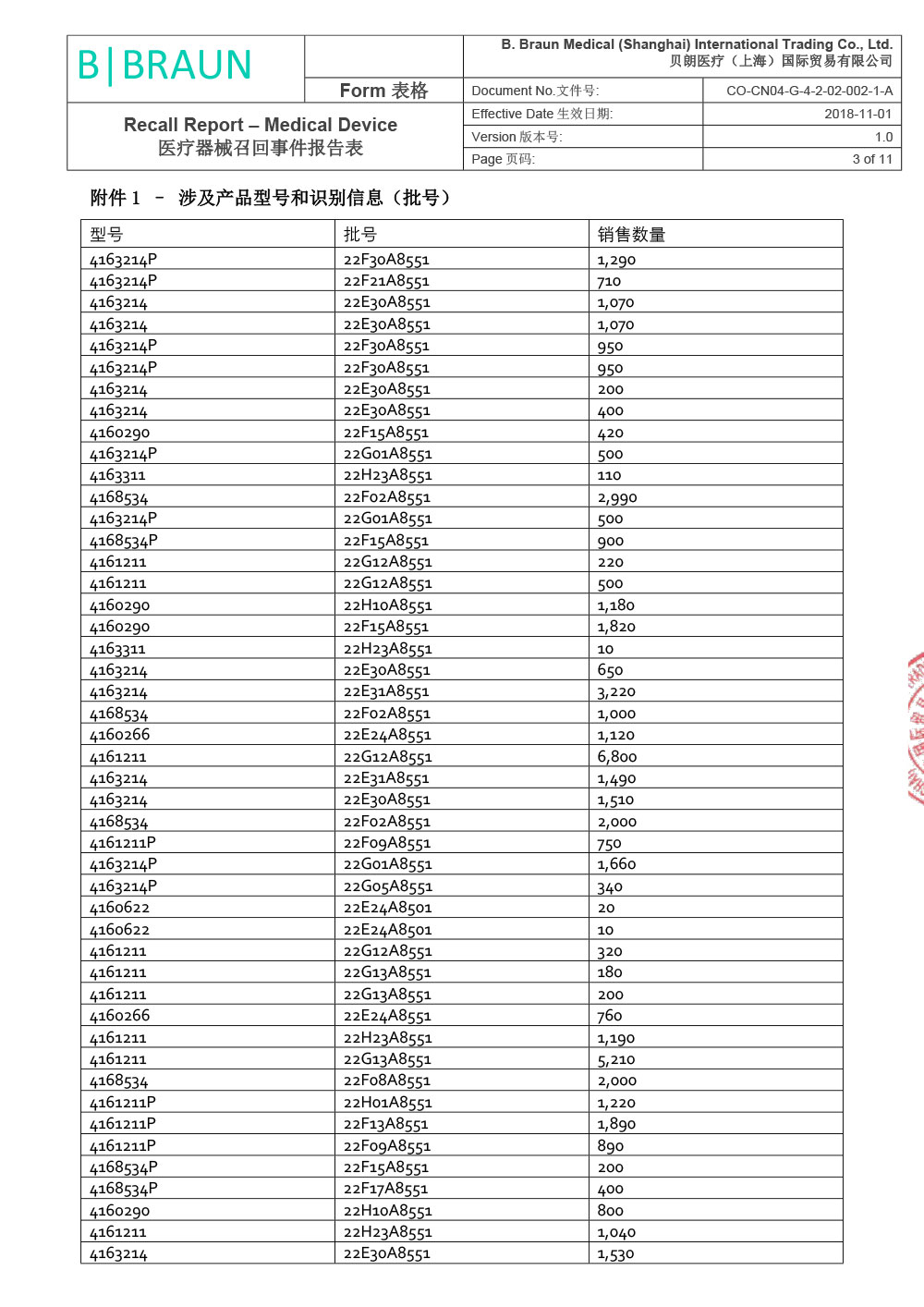
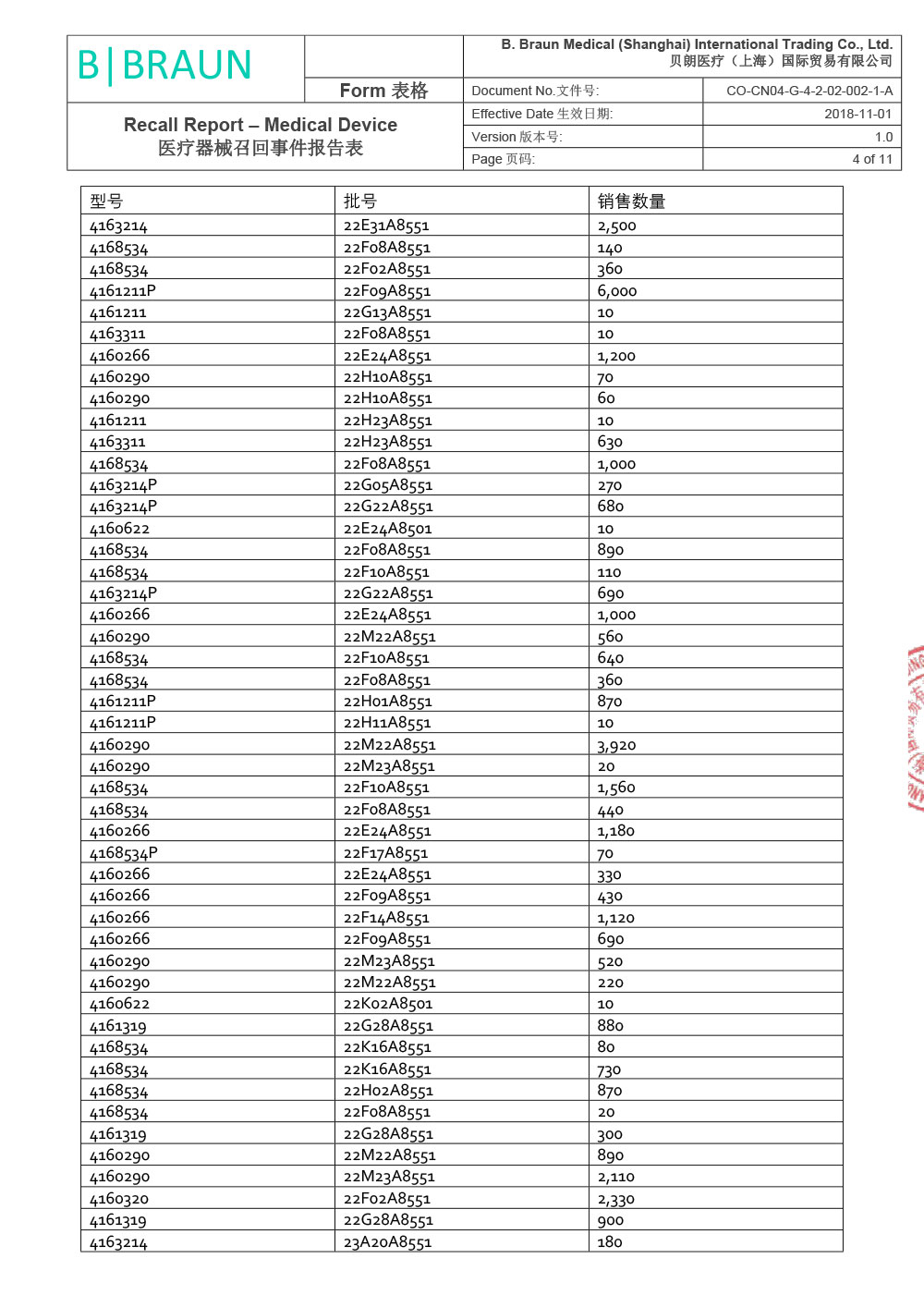
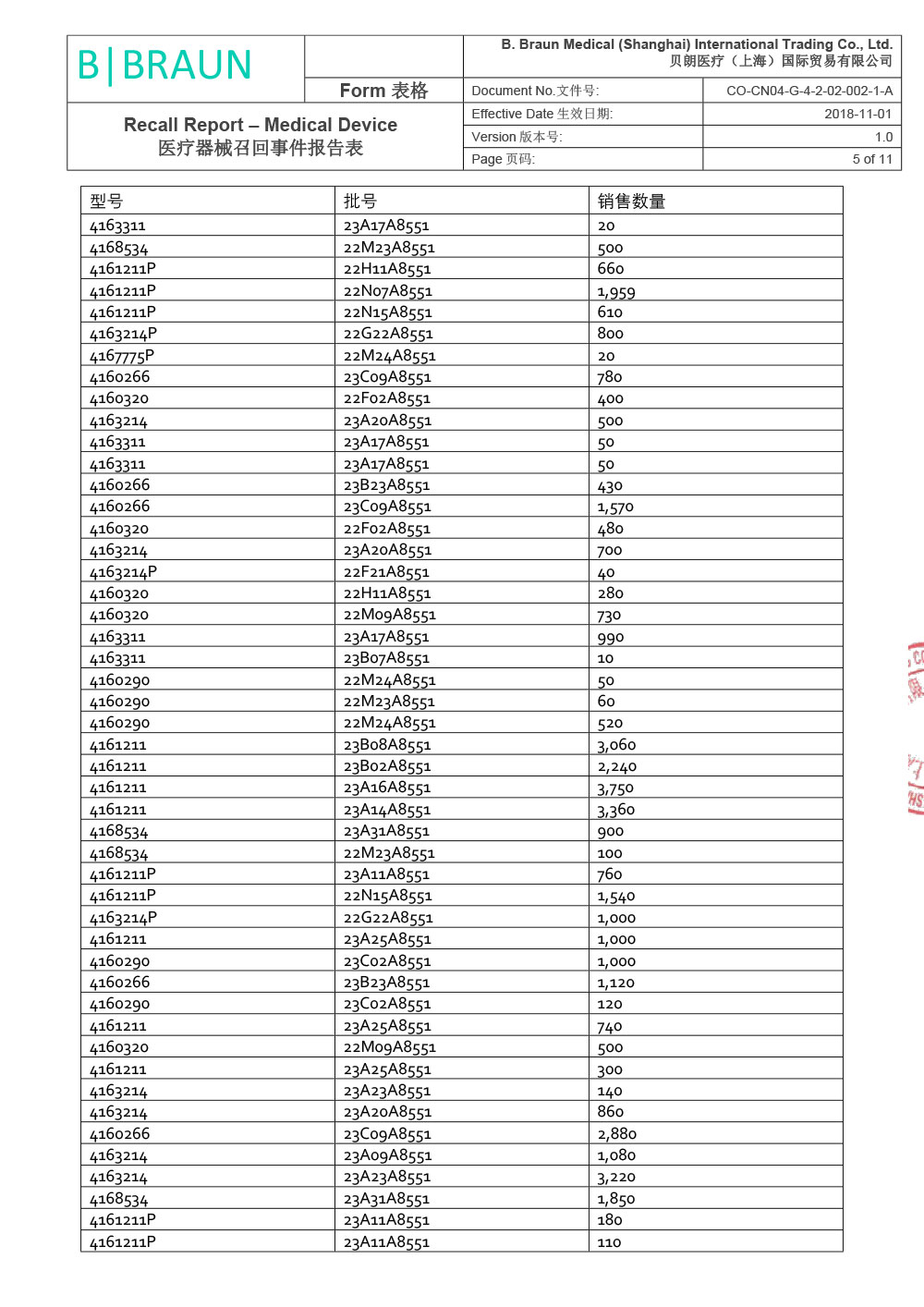
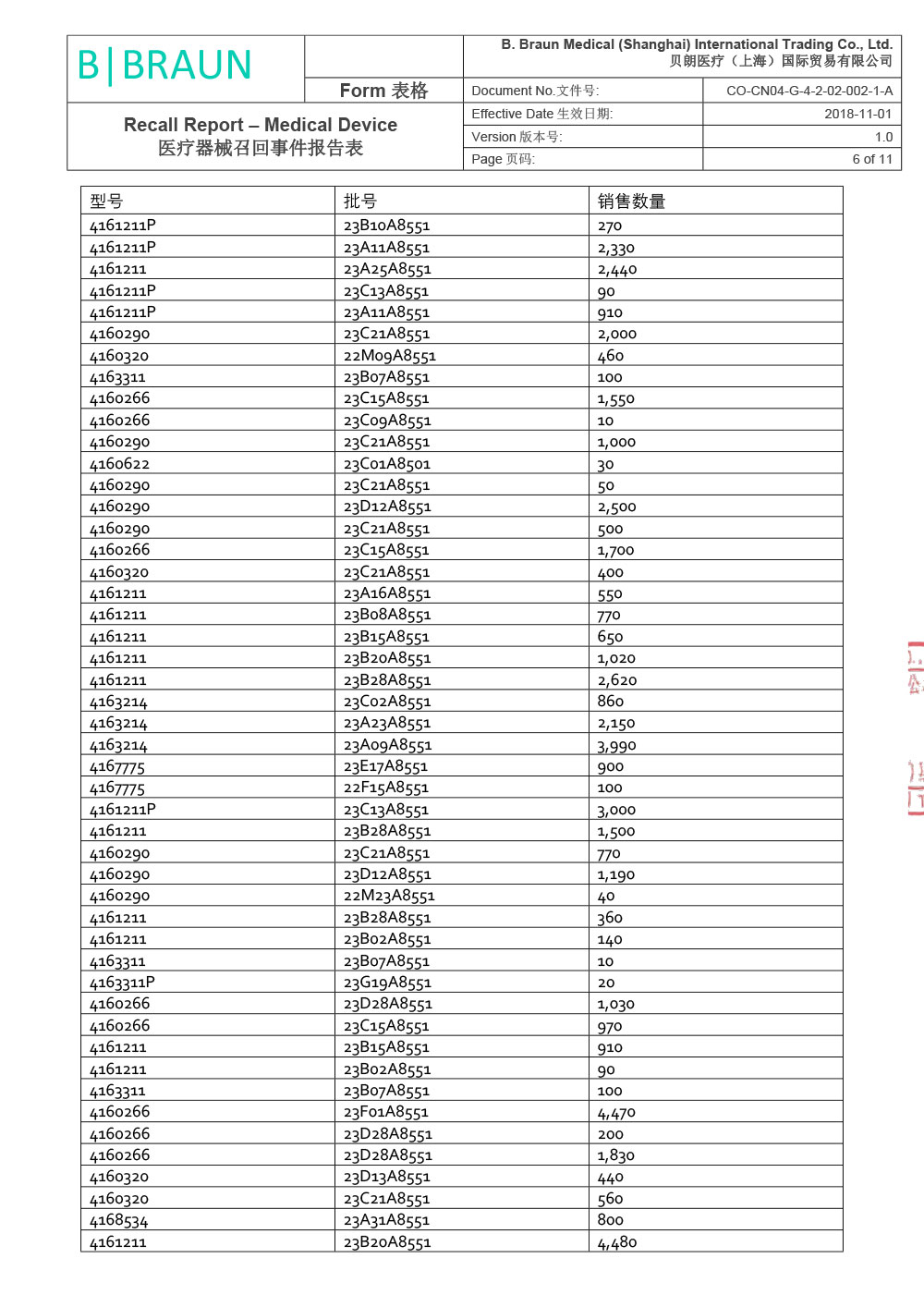
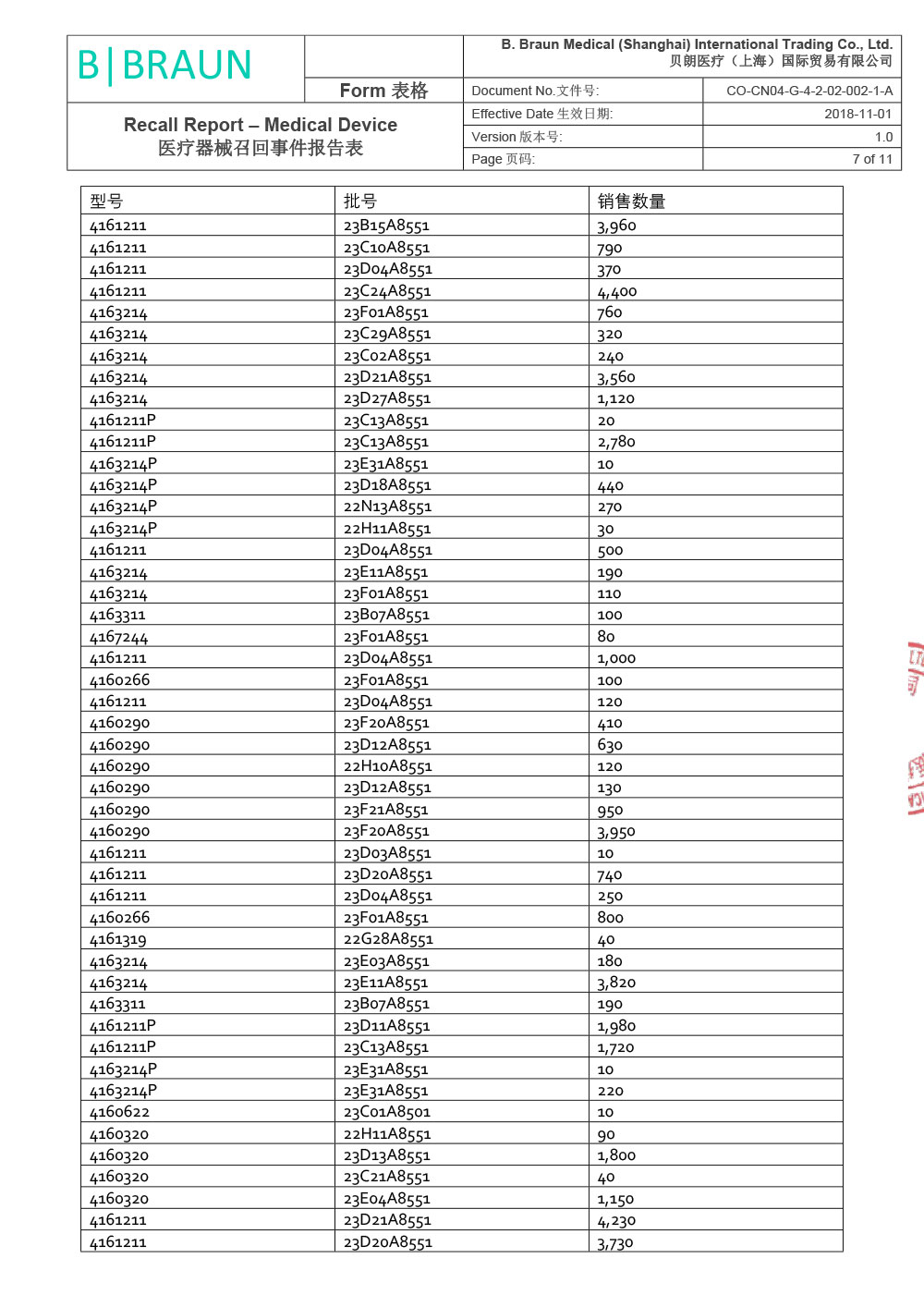
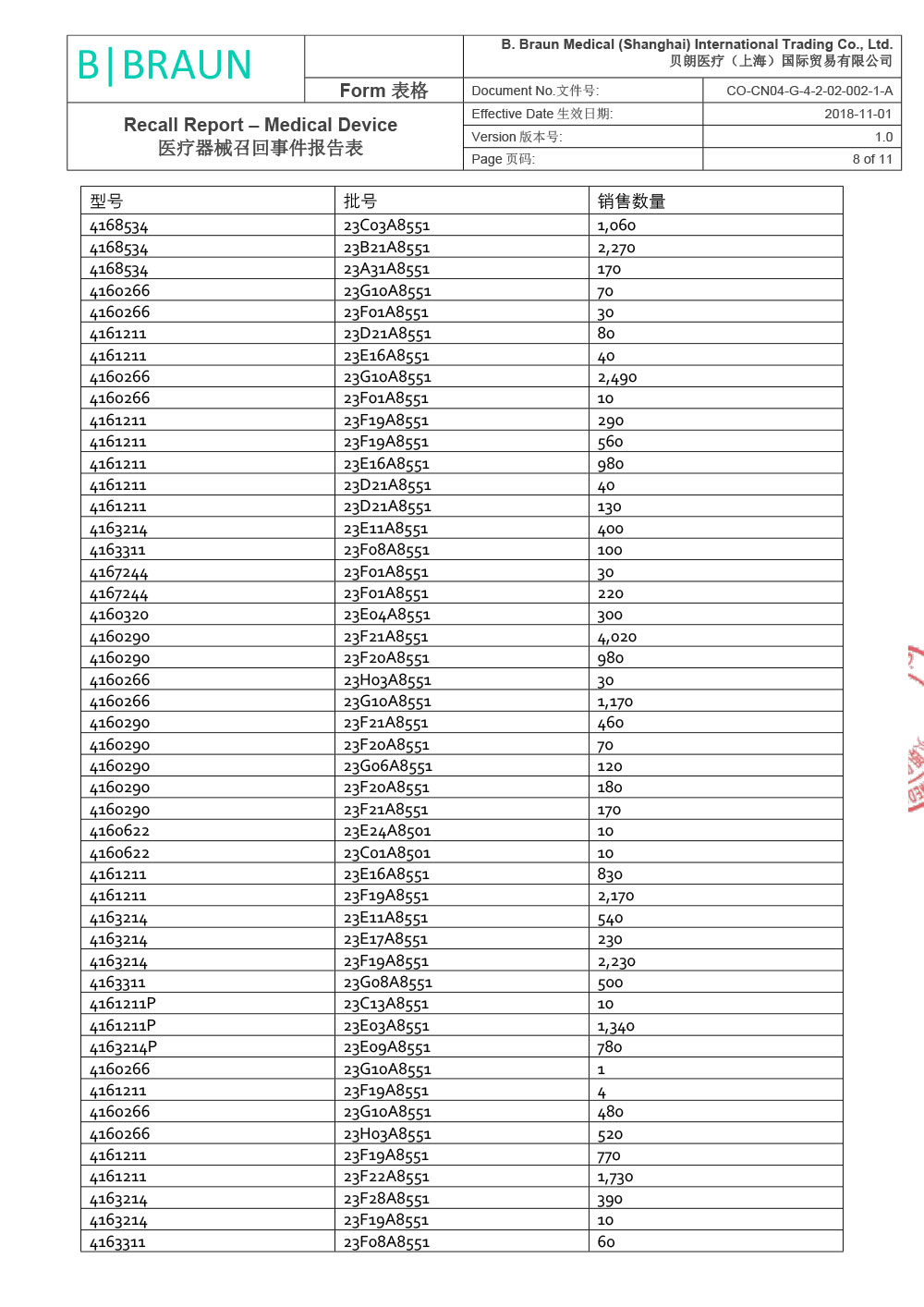
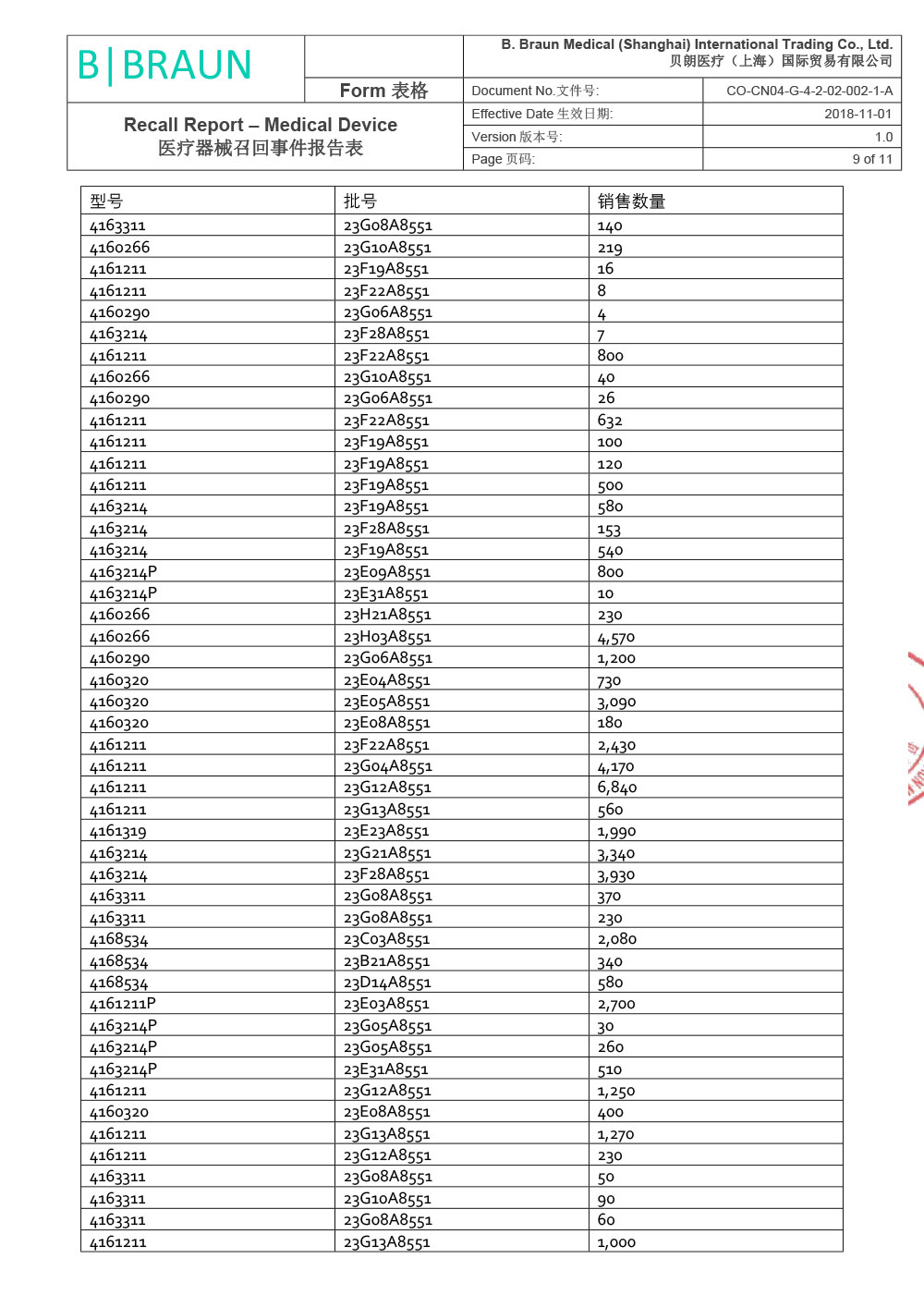
贝朗医疗(上海)国际贸易有限公司报告,由于涉及产品因生产商在上市后监测活动过程中经调查确定,组件8416275 - Y型导引针18GA(散装)(Certofix®和ProSet® Certofix产品的一部分)在其中一台注塑机上生产时使用了错误的螺纹。该组件用作导引针,可置入中心静脉导管(Certofix和ProSet Certofix)。 含有受影响组件的成品于2022年6月至2022年12月期间生产,并于2022年8月开始投放市场。 2022年11月,生产商首次收到有关螺纹问题的市场反馈,经调查找出了生产过程中出现的偏差,立刻采取纠正预防措施纠正了注塑工具的螺纹设置。根据ISO 14971标准,生产商随即进行了内部风险评定。 鉴于已识别的风险,为了确保临床使用的性能和便利性,生产商决定主动召回市场上受影响的器械。贝朗医疗(上海)国际贸易有限公司对其生产的一次性使用中心静脉导管包;中心静脉导管(注册证号:国械注进20153032561;国械注进20143035019)主动召回。召回级别为二级。涉及产品的型号、规格及批次等详细信息见《医疗器械召回事件报告表》。
2024年03月29日

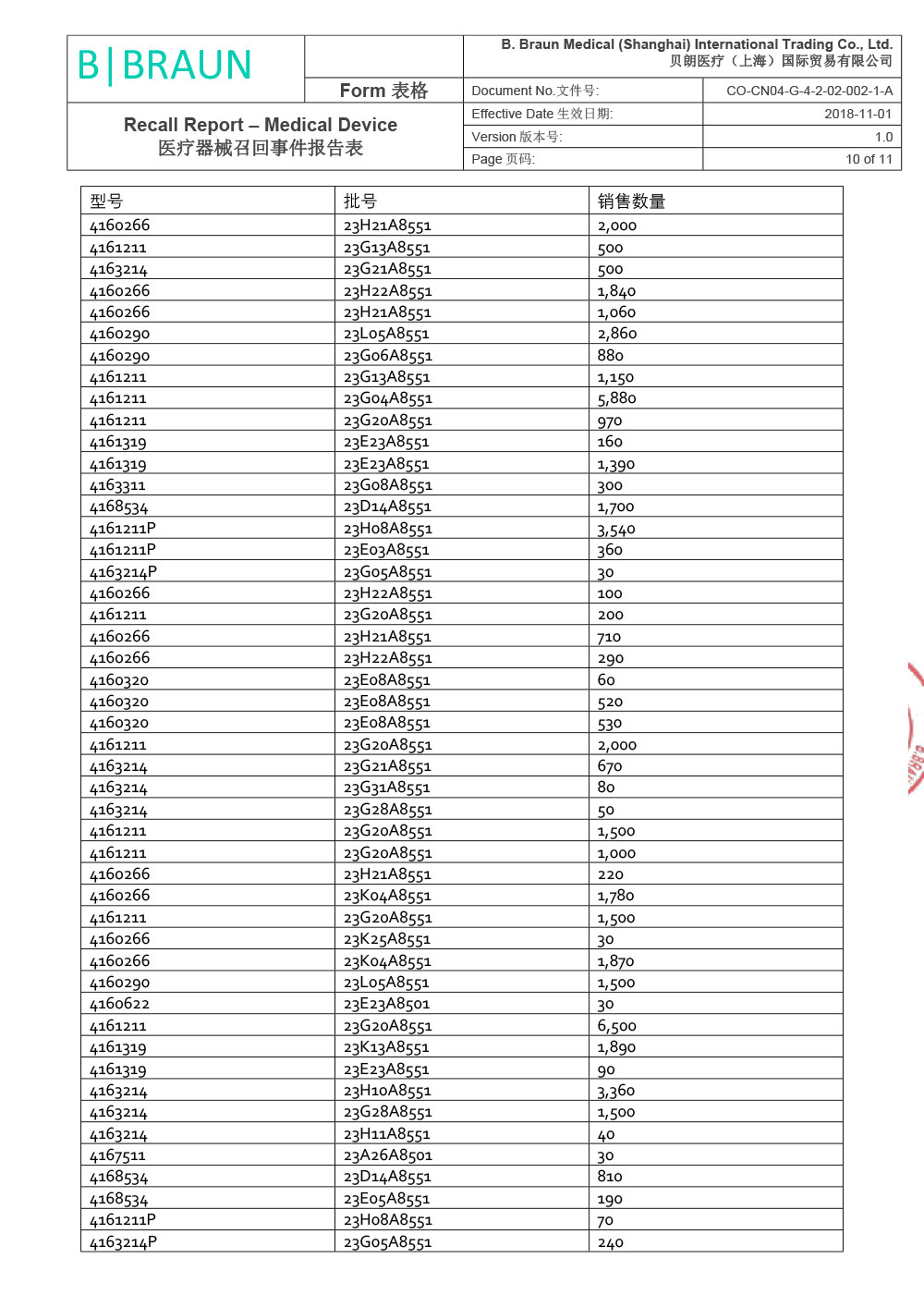
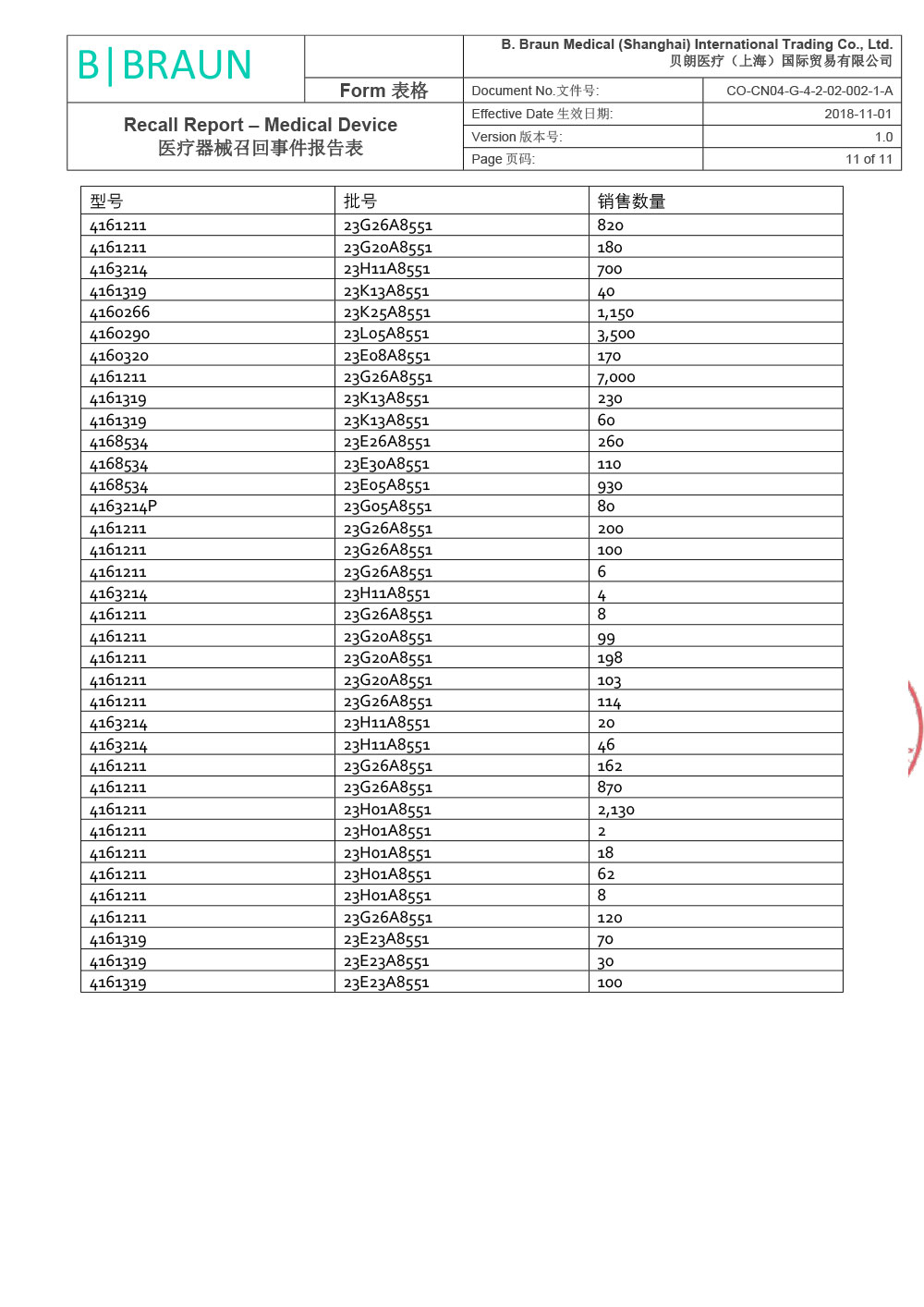
相关推荐
CIO提供以下相关文库下载、合规服务以及线上培训课程学习。
有疑问、问专家
提问
 E邀专家
E邀专家
手机桌面放:
合规导向小程序
法规同步、监管同频

最新推荐
上海市药品监督管理局关于注销光疗仪等5个医疗器械注册证书的通告 沪药监通告〔2026〕12号
2026-05-29
通用电气医疗系统贸易发展(上海)有限公司 对 多功能培养箱 主动召回 沪药监械主召2026-086
2026-05-29
美敦力(上海)管理有限公司 对 移动式O形臂X射线机 主动召回 沪药监械主召2026-085
2026-05-29
上海市西门子医疗系统有限公司 对 医用血管造影X射线机;医用血管造影X射线机X-ray Angiography System 主动召回 沪药监械主召2026-084
2026-05-27
波科国际医疗贸易(上海)有限公司 对 导丝导引球囊扩张导管 CRE Wireguided Balloon Dilatation Catheter;导丝导引球囊扩张导管 CRE Pro Wireguided Balloon Dilatation Catheter 主动召回 沪药监械主召2026-082
2026-05-27

药械企业法律风险预防与应对闭门会

执业药师继教服务

合规破局与价值重塑 医药营销转型实战训练营

药物警戒第三方委托服务

医药企业涉刑防范与应对

生死红线——「医改+反腐」背景下的医药企业生存逻辑与增长路径企业内训

药品医疗器械企业安全风险排查服务

【医药传播】药企品牌 / 产品宣传片制作

医疗器械注册/备案、变更

药品(国产/进口)注册、变更

药品经营许可申请 / 变更

化妆品生产许可申请/变更

医疗器械生产许可申请/变更

药品上市许可持有人的B证申请

药品生产许可申请 / 变更(药厂筹建)

原辅包注册/登记

化妆品注册/备案、变更

药械企业法律风险预防与应对闭门会

执业药师继教服务

合规破局与价值重塑 医药营销转型实战训练营

药物警戒第三方委托服务

医药企业涉刑防范与应对

生死红线——「医改+反腐」背景下的医药企业生存逻辑与增长路径企业内训
分享






