 E邀专家
E邀专家
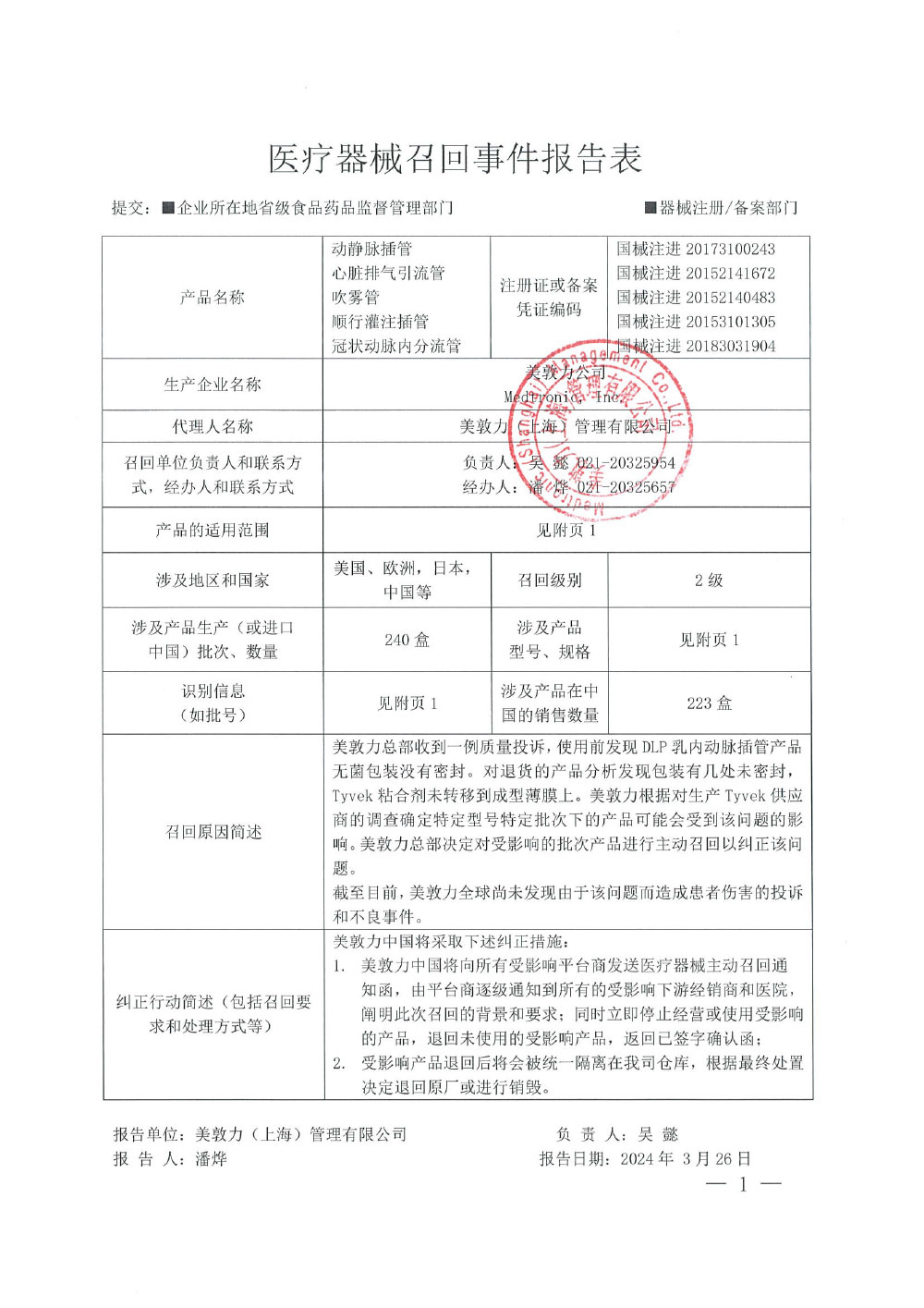
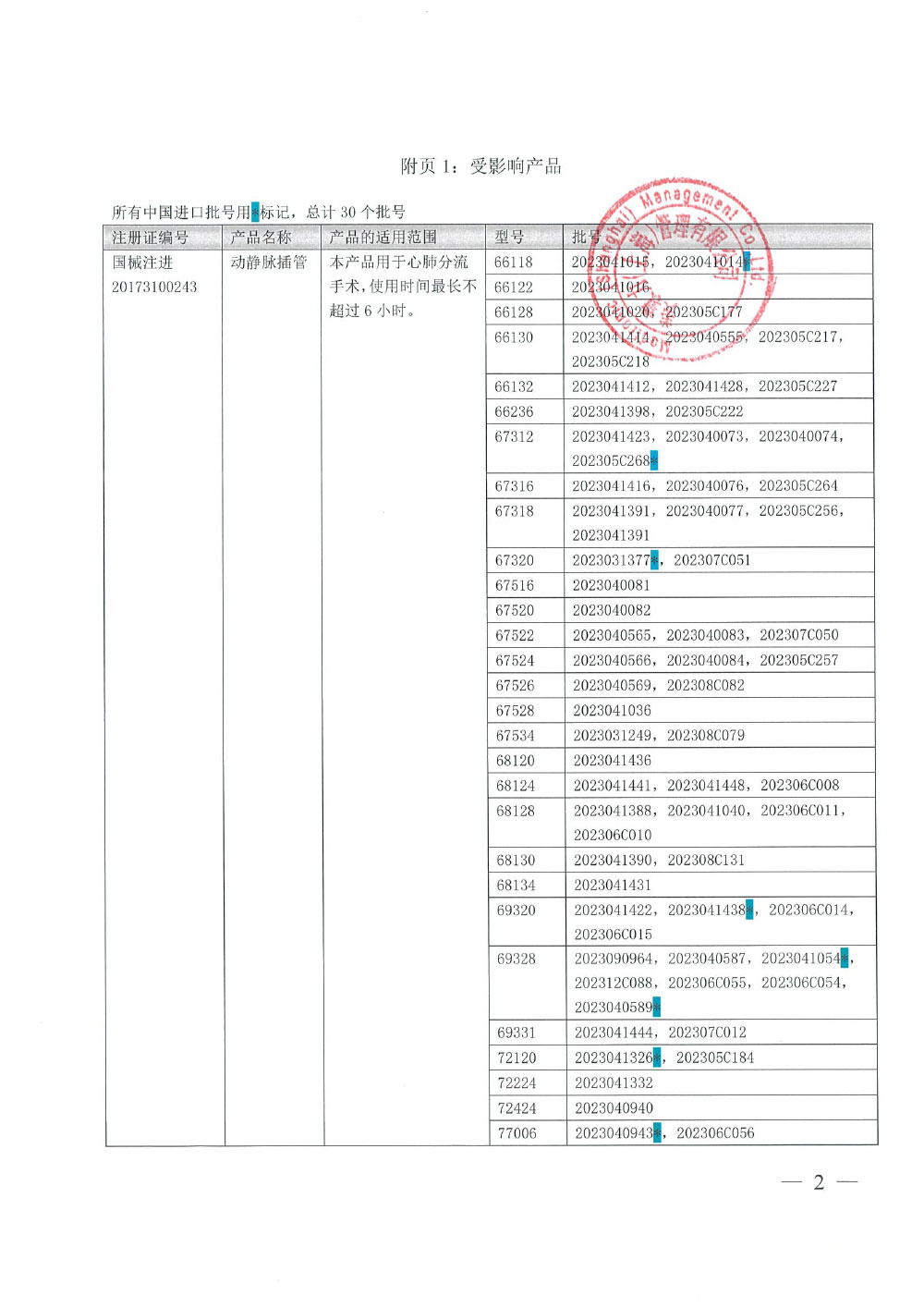
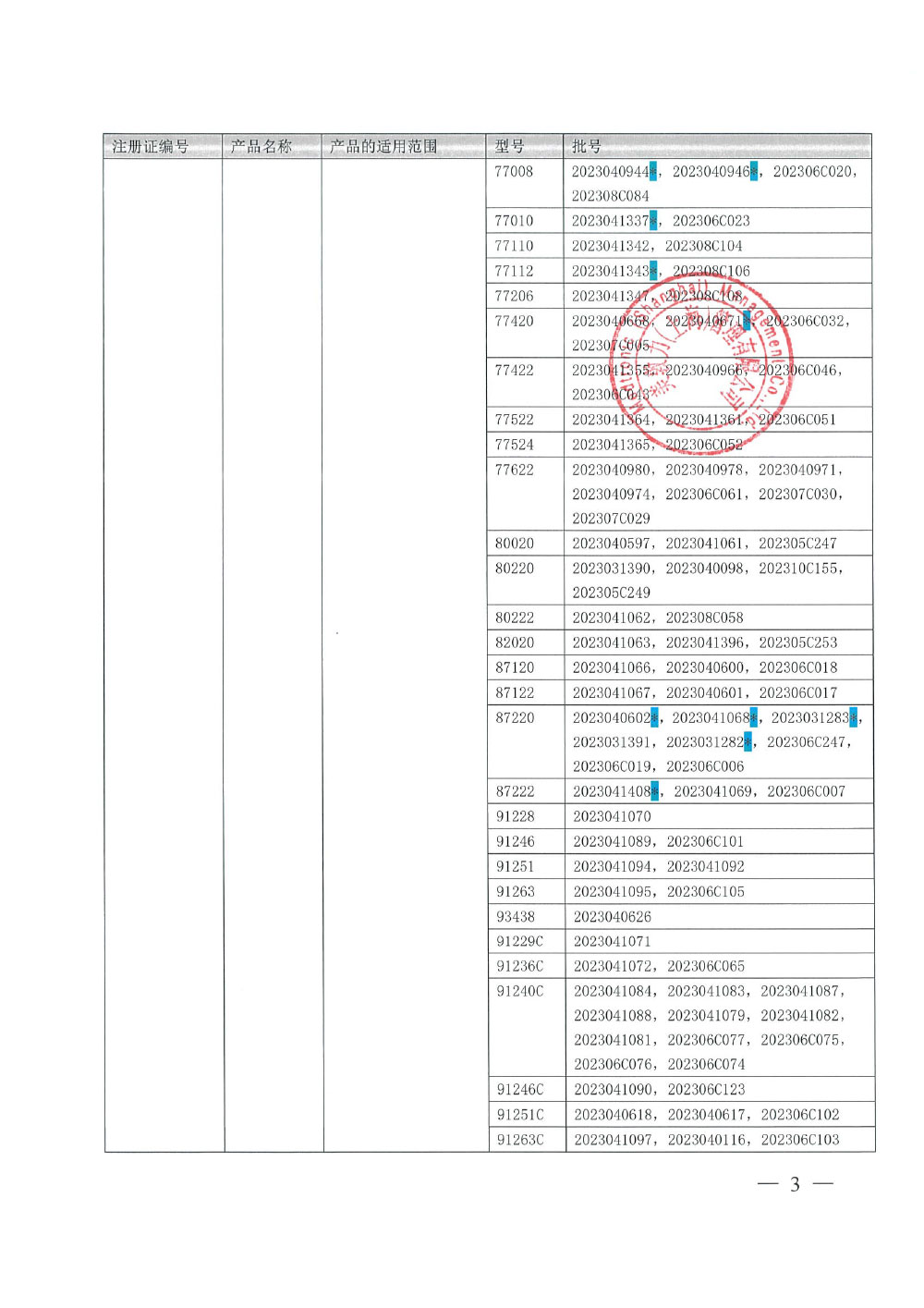
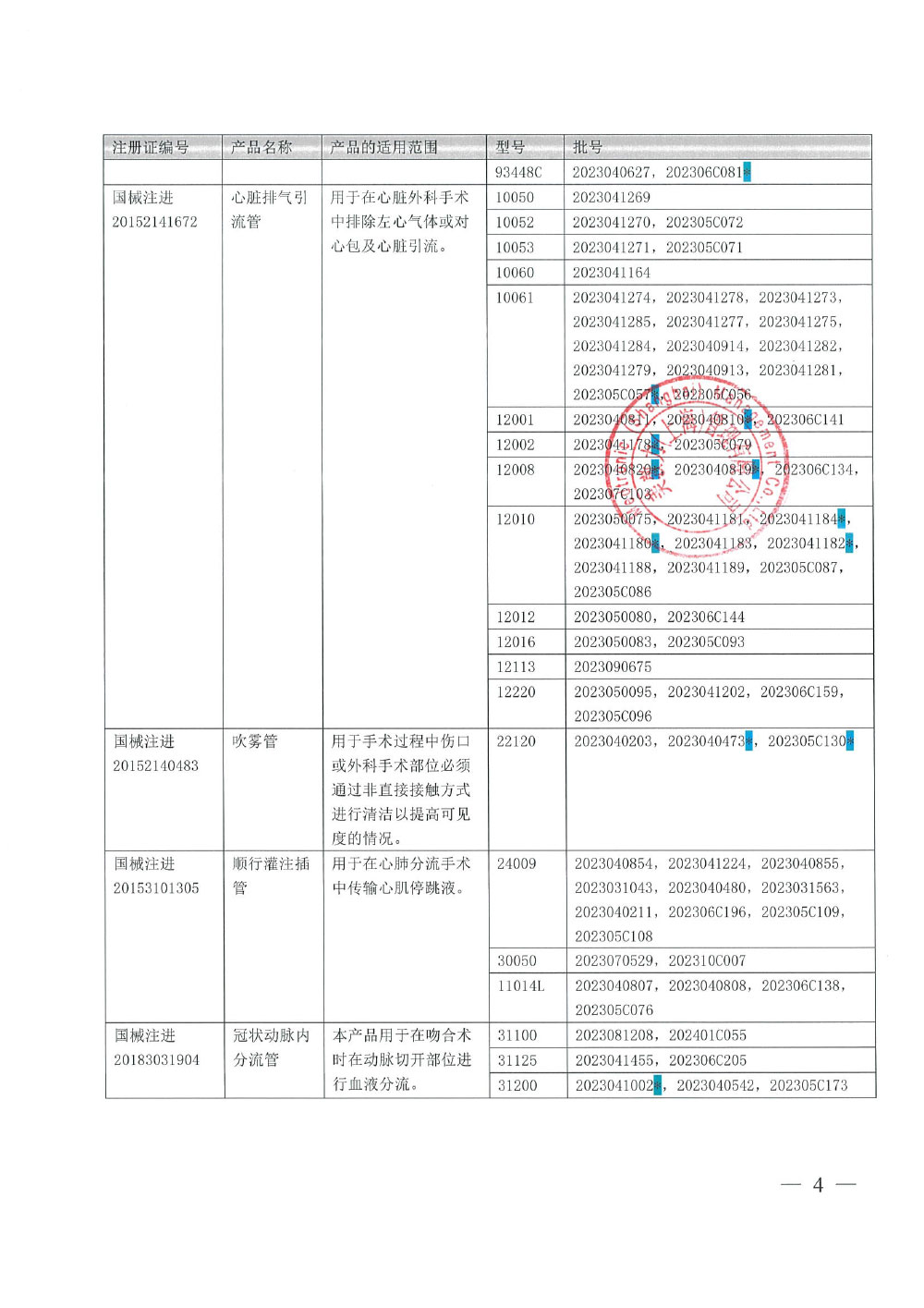
美敦力(上海)管理有限公司对动静脉插管、心脏排气引流管、吹雾管、顺行灌注插管、冠状动脉内分流管主动召回(沪药监械主召2024-065)
上海市 阅读 1960
收藏
美敦力(上海)管理有限公司报告,美敦力总部收到一例质量投诉,使用前发现DLP乳内动脉插管产品无菌包装没有密封。对退货的产品分析发现包装有几处未密封,Tyvek粘合剂未转移到成型薄膜上。美敦力根据对生产Tyvek供应商的调查确定特定型号特定批次下的产品可能会受到该问题的影响。美敦力总部决定对受影响的批次产品进行主动召回以纠正该问题。截至目前,美敦力全球尚未发现由于该问题而造成患者伤害的投诉和不良事件。生产商美敦力公司Medtronic, Inc.对其生产的动静脉插管(注册证号:国械注进20173100243),心脏排气引流管(注册证号:国械注进20152141672),吹雾管(注册证号:国械注进20152140483),顺行灌注插管(注册证号:国械注进20153101305)和冠状动脉内分流管(注册证号:国械注进20183031904)主动召回。召回级别为二级。涉及产品的型号、规格及批次等详细信息见《医疗器械召回事件报告表》。
2024年03月26日
相关推荐
CIO提供以下相关文库下载、合规服务以及线上培训课程学习。
有疑问、问专家
提问
 E邀专家
E邀专家
手机桌面放:
合规导向小程序
法规同步、监管同频

最新推荐
上海市药品监督管理局关于注销光疗仪等5个医疗器械注册证书的通告 沪药监通告〔2026〕12号
2026-05-29
通用电气医疗系统贸易发展(上海)有限公司 对 多功能培养箱 主动召回 沪药监械主召2026-086
2026-05-29
美敦力(上海)管理有限公司 对 移动式O形臂X射线机 主动召回 沪药监械主召2026-085
2026-05-29
上海市西门子医疗系统有限公司 对 医用血管造影X射线机;医用血管造影X射线机X-ray Angiography System 主动召回 沪药监械主召2026-084
2026-05-27
波科国际医疗贸易(上海)有限公司 对 导丝导引球囊扩张导管 CRE Wireguided Balloon Dilatation Catheter;导丝导引球囊扩张导管 CRE Pro Wireguided Balloon Dilatation Catheter 主动召回 沪药监械主召2026-082
2026-05-27

药械企业法律风险预防与应对闭门会

执业药师继教服务

合规破局与价值重塑 医药营销转型实战训练营

药物警戒第三方委托服务

医药企业涉刑防范与应对

生死红线——「医改+反腐」背景下的医药企业生存逻辑与增长路径企业内训

药品医疗器械企业安全风险排查服务

【医药传播】药企品牌 / 产品宣传片制作

医疗器械注册/备案、变更

药品(国产/进口)注册、变更

药品经营许可申请 / 变更

化妆品生产许可申请/变更

医疗器械生产许可申请/变更

药品上市许可持有人的B证申请

药品生产许可申请 / 变更(药厂筹建)

原辅包注册/登记

化妆品注册/备案、变更

药械企业法律风险预防与应对闭门会

执业药师继教服务

合规破局与价值重塑 医药营销转型实战训练营

药物警戒第三方委托服务

医药企业涉刑防范与应对

生死红线——「医改+反腐」背景下的医药企业生存逻辑与增长路径企业内训
分享






