 E邀专家
E邀专家
2021年至今因违反GMP非法经营的药企已有4位法定代表人、2位质量负责人被10年禁业
甘肃省药品监督管理局发布2020年药品医疗器械五大典型案例。张掖市恒利中药材加工有限公司生产销售劣药案,武威市康泰堂药业有限公司生产销售假药案,依法作出吊销《药品生产许可证》、法定代表人、质量负责人十年内不得从事药品生产经营活动的行政处罚。

1:张掖市恒利中药材加工生产销售劣药,法定代表人十年内禁业
2019年6月20日,甘肃省药品稽查局根据群众举报,对张掖市恒利中药材加工有限公司进行检查。经查,当事人存在生产销售劣药中药饮片地骨皮、海风藤,以及未按规定实施《药品生产质量管理规范(2021年修订)》的违法行为。违反了《中华人民共和国药品管理法》(2015年修正)第九条第一款、第三十二条第一款、第四十九条第一款的规定。依据《中华人民共和国药品管理法》(2015年修正)第七十四条、第七十八条、第七十五条第一款之规定,对当事人依法给予没收劣药、没收违法所得34966.16元、罚款128508.24元、吊销《药品生产许可证》、法定代表人十年内不得从事药品生产、经营活动的行政处罚。
2:武威市康泰堂药业生产销售假药,法定代表人和质量负责人十年内禁业
2020年6月18日,甘肃省药品监督管理局生产监督管理处根据武威市市场监督管理局报告,对武威市康泰堂药业有限公司立案调查。经查,当事人2014年至2019年期间因生产销售假药被武威市凉州区人民法院3次作出有罪判决,2013年至2014年期间因生产销售假药和多次违反《药品生产质量管理规范》被原武威市食品药品监督管理局5次给予行政处罚。当事人违反了《中华人民共和国药品管理法》(2015年修订)第四十八条第一款、第九条第一款的规定。依据《药品管理法》第七十三条、第七十五条、第七十八条的规定和《食品药品行政执法与刑事司法衔接工作办法》第十五条等规定,依法对其作出吊销《药品生产许可证》、法定代表人和质量负责人十年内不得从事药品生产经营活动的行政处罚。

3、江苏普华克胜药业法定代表人有组织地使用未经批准原料药违法生产药品销售,法定代表人十年内禁业。
2021年4月20日,江苏省药监局发布了《行政处罚听证告知书》送达公告。经查,2016年11月至2019年3月江苏普华克胜药业有限公司使用未经批准的原料药违法生产药品并销售。期间,杨华担任该公司法定代表人,有组织地推动实施上达述违法生产、销售活动。被处十年内不得从事药品生产、经营活动。
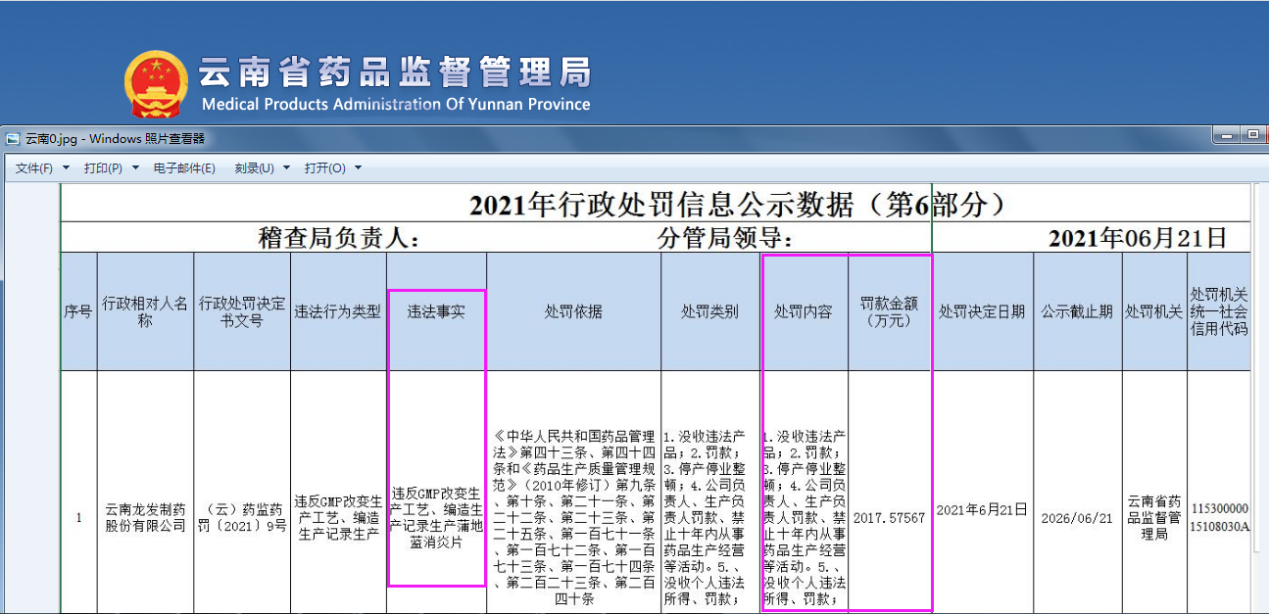
4、云南龙发制药股份有限公司违反GMP改变生产工艺、编造生产记录生产蒲地蓝消炎片,公司负责人、生产负责人十年内禁业。
2021年6月25日,云南省药监局公示一则行政处罚信息,云南龙发制药股份有限公司违反GMP改变生产工艺、编造生产记录生产蒲地蓝消炎片。被没收违法产品;停产停业整顿;被罚款2017.57567万元;公司负责人、生产负责人罚款、禁止十年内从事药品生产经营等活动。
5、曲靖鸿源中药饮片未遵守《药品生产质量管理规范》从事药品生产,法定代表人十年内禁业。
今年5月,云南省药监局公布了2021年一则行政处罚信息公示,曲靖鸿源中药饮片有限公司被人举报,称曲靖鸿源中药饮片有限公司未按药品生产质量管理规范要求从事中药饮片生产,生产过程无批生产记录和检验报告,生产的中药饮片未经检验直接上市销售。经查该公司提供不出2019年的59批次、2020年的9批次中药饮片的批生产记录,生产所用原料、生产过程和生产参数等信息无法追溯。
该公司2015年3月首次通过药品GMP认证至今,质量负责人和质量受权人历经肖家宝、熊堃、李有才、汤智钧和张祎,生产负责人历经申建、佟刚连、王卖丽和刘倩,企业关键岗位人员变更频繁,现有人员除法定代表人和企业负责人王玉伟外,均为近期陆续新招聘人员,公司人员流动大。该公司仅提供得出刘倩的备案件,其它人员备案件均提供不出。
被吊销曲靖鸿源中药饮片有限公司《药品生产许可证》;对法定代表人王玉伟十年内禁止从事药品生产经营等活动。"
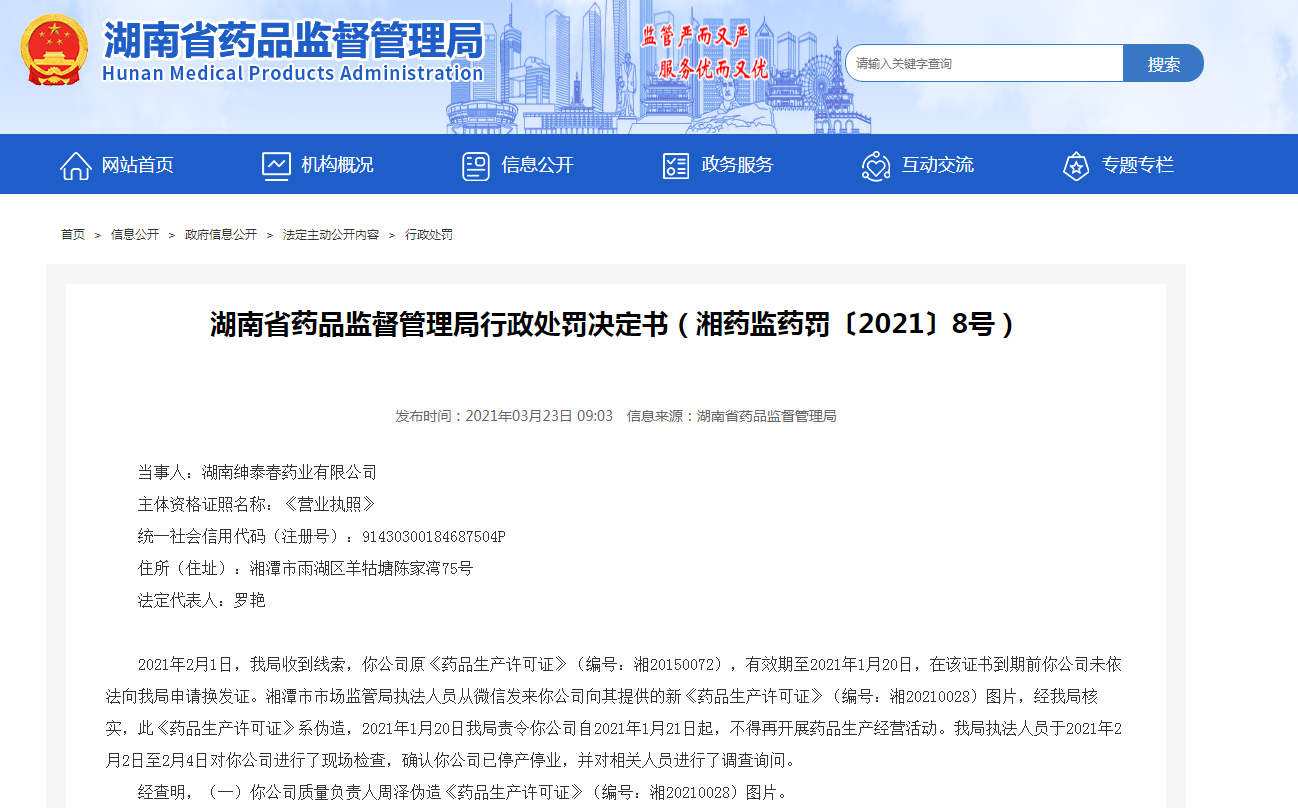
6、质量负责人“PS”生产许可证,被十年禁业
2021年3月23日,湖南省药监局发布了行政处罚决定书,决定书显示:湖南绅泰春药业有限公司在多次会议上进行了安排布置和督促督办许可证换证,周泽每次会上都说在办,但因其个人原因,对自身职责认识不够,且换证申报资料未准备好,一直未到湖南省药监局办理换证事宜。
2021年1月12日,周泽先在网吧自己制作了一张《药品生产许可证换发证受理通知单》电子图片并打印一张纸质件交给了你公司销售部经理肖勇;1月15日,周泽在网吧又制作了两张《药品生产许可证》(编号:湘20210028)电子图片,一张黑白、一张彩色,均通过微信发给你公司销售部经理肖勇。
公司法定代表人处十万元罚款。原质量负责人周泽以下行政处罚:1.处十万元罚款;2.十年禁止从事药品生产经营等活动。
相关推荐
CIO提供以下相关文库下载、合规服务以及线上培训课程学习。
 E邀专家
E邀专家

最新推荐

药械企业法律风险预防与应对闭门会

执业药师继教服务

合规破局与价值重塑 医药营销转型实战训练营

药物警戒第三方委托服务

医药企业涉刑防范与应对

生死红线——「医改+反腐」背景下的医药企业生存逻辑与增长路径企业内训

药品医疗器械企业安全风险排查服务

【医药传播】药企品牌 / 产品宣传片制作

医疗器械注册/备案、变更

药品(国产/进口)注册、变更

药品经营许可申请 / 变更

化妆品生产许可申请/变更

医疗器械生产许可申请/变更

药品上市许可持有人的B证申请

药品生产许可申请 / 变更(药厂筹建)

原辅包注册/登记

化妆品注册/备案、变更

药械企业法律风险预防与应对闭门会

执业药师继教服务

合规破局与价值重塑 医药营销转型实战训练营

药物警戒第三方委托服务

医药企业涉刑防范与应对

生死红线——「医改+反腐」背景下的医药企业生存逻辑与增长路径企业内训






