
原辅包GMP符合性审计
1.对企业的质量体系执行情况进行审查。 2.帮助企业及时发现不规范质量行为及潜在隐患。 3.评定企业的质量管理体系水平。 4.给出纠正预防措施的建议。
参考价格 ¥0.00 ¥0.00


原辅包GMP符合性审计相关法规要求
《药品管理法》第四十五条规定“生产药品所需的原料、辅料,应当符合药用要求、药品生产质量管理规范的有关要求”。
《药品生产质量管理规范》 第一百二十条规定“与药品直接接触的包装材料和印刷包装材料的管理和控制要求与原辅料相同”。
原辅包GMP符合性审计的必要性
药厂供应商常常被药品生产企业要求提供GMP符合性证据,以便药品生产企业通过GMP符合性评估来了解企业质量体系情况,便于后期进行质量控制。
当被合作伙伴要求提供GMP符合性证明时,药厂供应商通常有两种方式。一是企业自行建立和运行GMP之后宣称符合;二是邀请专业第三方机构评估,出具GMP符合性审计证书。后者更加客观真实,避免走过场、编报告,同时第三方机构丰富的检查经验,更能帮助企业发现自身潜在的合规风险,审计报告更有说服力。
我们的服务
CIO合规保证组织按照审计程序要求,依据原辅包相关法规的要求对企业进行质量体系的全面审计(包括:公用设施、生产车间、仓库、检验室现场,确认与验证,质量体系文件与记录等),审计过程中与企业人员进行沟通交流,审计后出具全面系统的审计报告,列出风险点,评价风险级别,提出整改建议。
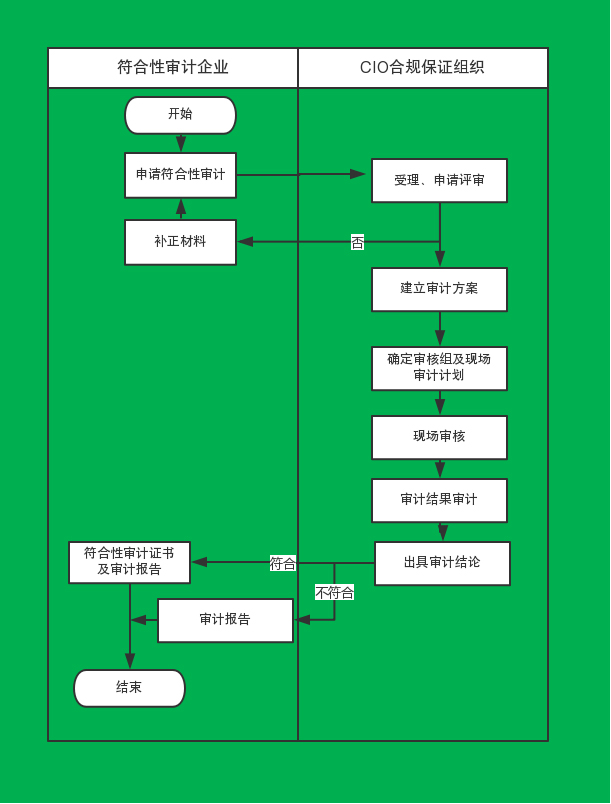
服务流程
服务对象
药品生产企业、药品研发机构、药物中间体工厂、原料药工厂、药用辅料工厂、药包材工厂等需要第三方审计,评估其GMP符合性的企业。
证书模板

我们的优势

热门推荐
分享









