I期临床研究全程质量控制体系管理培训班暨I期药物临床试验论坛

为配合仿制药一致性评价工作的有序开展,助力我省生物医药创新发展,广东省药学会、东莞市人民医院于2017年成功举办I期药物临床试验室建设与管理培训班暨第一届I期临床试验东莞论坛,截止目前,全省已有20家I期临床试验中心陆续建成投入使用。为进一步提高I期临床试验运行管理以及研究项目质量,强化I期临床试验规范化操作,促进I期临床试验管理水平的提高,有效保障受试者的安全和权益,在广东省药学会的指导下,东莞市人民医院将于8月11-12日举办I期临床研究全程质量控制体系管理培训班暨第二届I期临床试验东莞论坛。本次培训班及论坛主要面向I期临床试验室研究人员及伦理委员会人员、药物研发机构或药品生产企业研发人员、CRO及SMO公司的CRA、CRC。(提示:在线报名后可下载会议红头文件和会议日程)
一、培训时间:报到时间:8月10日14:30-18:00报到(会场附近的代表可以在8月11日8:30 前在会场门口报到),2018年8月11日-8月12日培训。
二、培训地点:东莞市万江区万道路南3号东莞市人民医院体检中心三楼会议室。
三、培训主题:I期临床研究全程质量控制体系管理。
四、培训方式:邀请国内、省内在I期药物临床试验运行管理及质量控制等方面有丰富经验的专家授课。
五、培训对象:I期临床试验研究人员及伦理委员会人员,药物研发机构或药品生产企业研发人员,CRO及SMO公司的CRA、CRC。
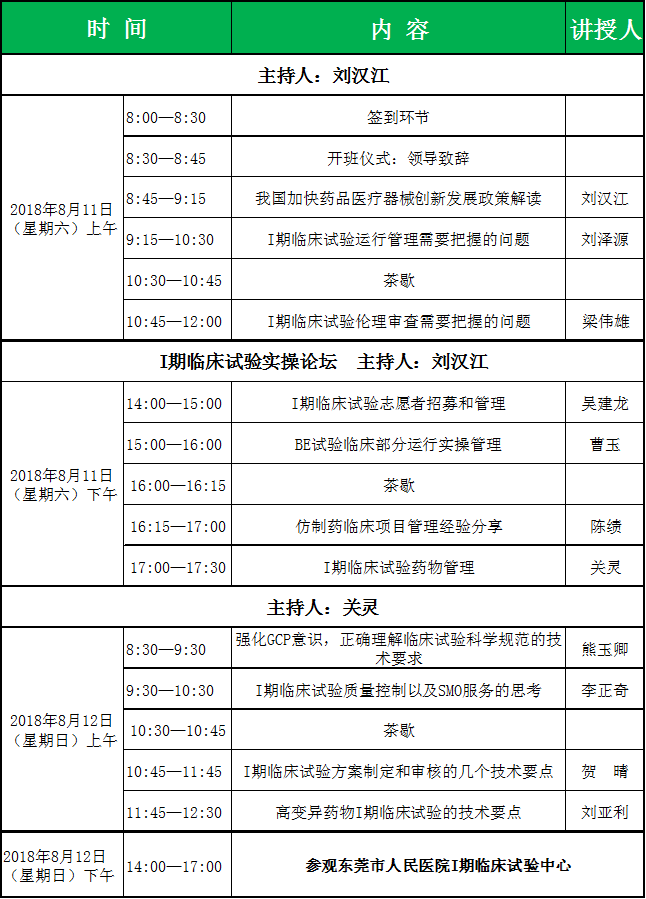
六、培训内容:
1、I期临床试验运行管理需要把握的问题(刘泽源教授)
2、强化GCP意识,正确理解临床试验科学规范的技术要求(熊玉卿教授)
3、I期临床试验质量控制以及SMO服务的思考(李正奇主任)
4、I期临床试验伦理审查需要把握的问题(梁伟雄教授)
5、I期临床试验方案制定和审核的几个技术要点(贺晴主任)
6、BE试验临床部分运行实操管理(曹玉主任)
7、I期临床试验志愿者招募和管理(吴建龙教授)
8、高变异药物I期临床试验的技术要点(刘亚利主任)
9、I期临床试验药物管理(关灵主任)
七、其 他:
1、报名方式
(1)二维码报名(推荐):请在8月5日前扫描下方二维码填写信息后提交即可报名。

电脑上网报名路径(推荐):
访问CIO在线(www.ciopharma.com)——“合规培训”
或者直接输入网址:
http://www.ciopharma.com/Pc/Train/FindTrainInfo/id/75
2、注册缴费:注册费1000元/人(要开发票须提供单位税务号码)
付款方式:(1)微信付款(推荐),填开票信息;
(2)现场缴费;
(3)银行转账
(账号:3602840409100325717,开户名:广东省医药合规促进会,开户行:中国工商银行广州福今支行),转账请注明“I期培训班+姓名”,发票及广东省药学会培训证书通过快递寄出。
3、交通食宿费用自理,附近住宿酒店推荐(请自行联系住宿)
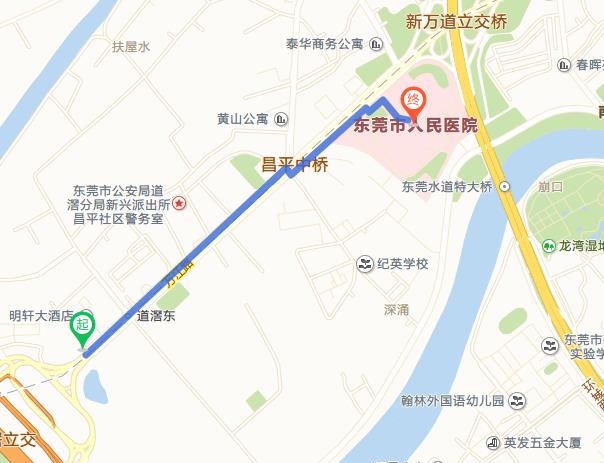
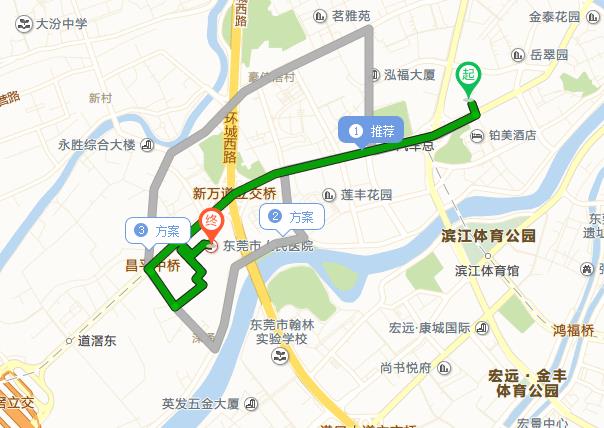
1)东莞市南华国际酒店(东莞市万江区滨江西路,毗邻阳光海岸,春晖园)电话:4001848220-886657)(离医院约1公里,步行约15分钟)。住宿参考价:单人房(大床)398元/天,标准双人房(双床)450元/天,含早餐。
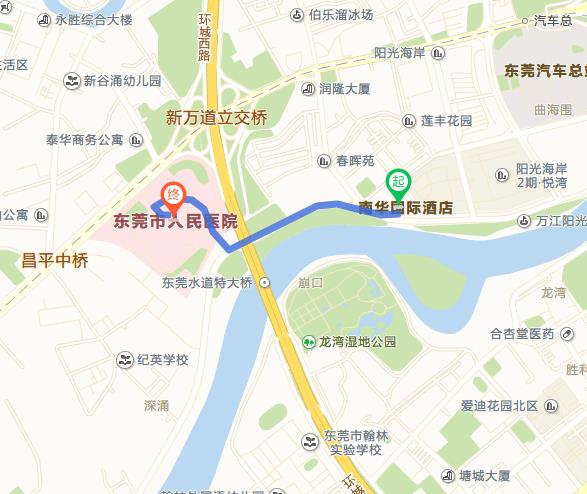
2)东莞市明轩大酒店(东莞市道滘镇广深高速公路道滘出入口旁,电话:0769-88333888)(离医院约2公里)。住宿参考价:豪华单人房:310元/天,豪华双人房:330元/天,含早餐。
3)锦江之星(东莞麦德龙店)(东莞市万江区金鳌大道北1号麦德龙商场院内,电话:0769-22183258)(离医院约3公里)。住宿参考价:标准房180元/天、219元/天,商务房218元/天、219元/天,不含早餐。
4、本次“I期临床研究全程质量控制体系管理培训班”为2018年国家级继续医学教育项目I类4分。
5、指导单位:广东省药学会
主办单位:东莞市人民医院
承办单位:广东省医药合规促进会
6、联系方式:
广东省医药合规促进会:
方经理:13632407611
陆先生:13925117001
培训课程
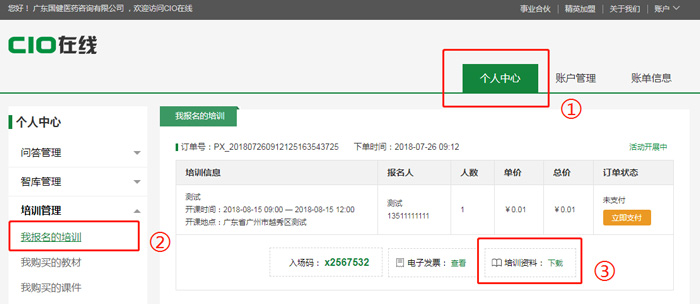
培训资料下载
报名成功后,点击企业中心→个人中心→我报名的培训→培训资料下载