
体外诊断试剂注册证变更
1.CIO为境内三类体外诊断试剂医疗器械注册、生产、经营提供全方位、一站式的医疗器械咨询办理服务。 2.CIO提供体外诊断试剂注册变更、延续服务,一次性通过快速拿证。
参考价格 ¥0.00 ¥0.00
体外诊断试剂注册证变更法规要求
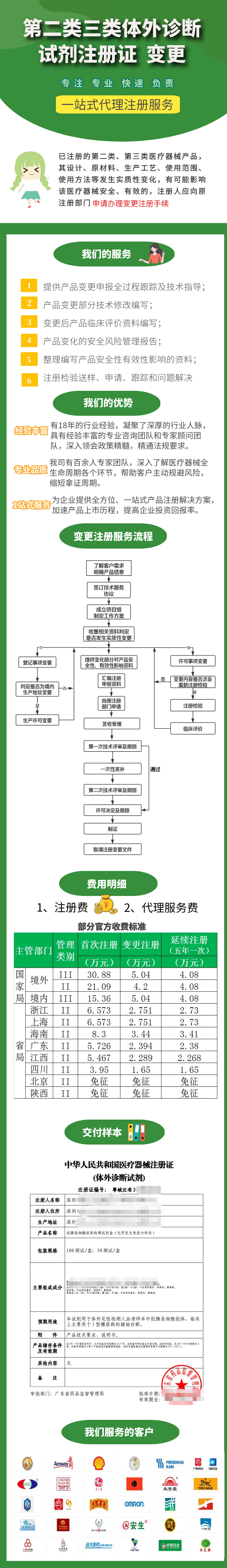
已注册的第二类、第三类医疗器械产品,其设计、原材料、生产工艺、使用范围、使用方法等发生实质性变化,有可能影响该医疗器械安全、有效的,注册人应向原注册部门申请办理变更注册手续。
体外诊断试剂注册证变更服务内容
提供产品变更申报全过程跟踪及技术指导;
产品变更部分技术修改编写;
变更后产品临床评价资料编写;
产品变化的安全风险管理报告;
整理编写产品安全性有效性影响的资料;
注册检验送样、申请、跟踪和问题解决
体外诊断试剂注册证延续服务流程
了解客户需求,明确产品信息——签订技术服务协议——成立项目组制定工作方案——收集相关资料判定是否发生实质性变更——提供变化部分对产品安全性、有效性影响资料——汇编注册申报资料——向原注册部门申请——签收受理——第一次技术评审及跟踪——一次性发补——第二次技术评审及跟踪——许可决定及跟踪——制证——取得注册变更文件
热门推荐
分享






