


医疗器械分类界定向哪个部门申请
医疗器械分类界定向所在地省药品监督管理部门申请,由省药品监督管理局综合判定后可以确定的直接出具意见,不确定的出具预分类意见,报国家局审核。
什么情况下需要医疗器械分类界定
1.产品类似医疗器械,但想按普通电子产品销售
2.产品是电子产品,但想作为医疗器械销售
3.新研制产品尚未列入分类目录
4.国外进口/港澳台生产的产品想在国内销售
5.药械组合产品的属性界定
医疗器械分类界定您需要关注以下问题
1.对新研制的尚未列入分类目录的医疗器械, 申请人可以直接按第三类医疗器械产品注册申请, 或者申请医疗器械分类界定。
2.拟生产的医疗器械在《医疗器械分类目录》及分类补充规定文件中无对应的品种, 或者企业依据上述规定文件不能自行判断类别, 可以申请医疗器械分类界定。
医疗器械分类界定服务内容
整理医疗器械分类界定申报资料
向药品监督管理部门申请分类
跟进审批过程,及时补充资料
协助企业取得分类结果
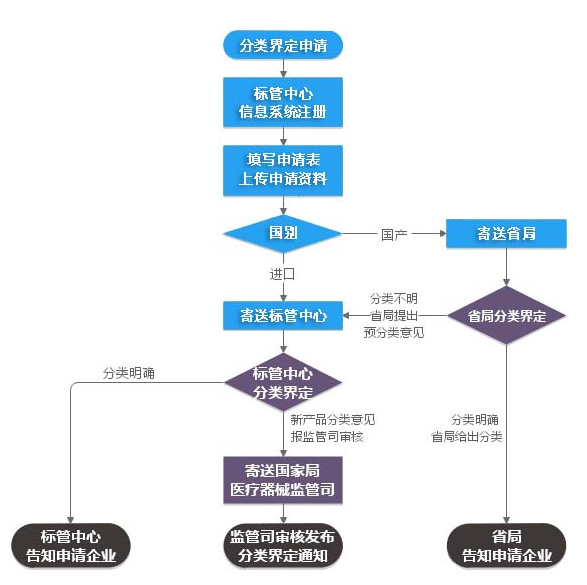
医疗器械分类界定服务流程
分享










